题目内容
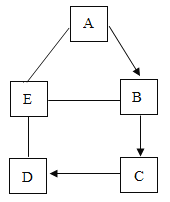
【题目】尿素[化学式为CO(NH2)2]是常用的化肥,制取尿素的反应微观示意图如图。
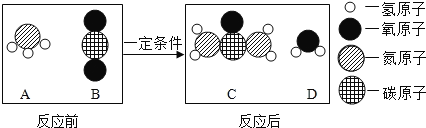
(1)该化学反应中A、B、C、D四种物质的分子个数比为_____;
(2)A、B、C、D四种物质中属于氧化物的是____(写化学式)
(3)一个A分子是由______构成的;
(4)上述反应中,不发生改变的粒子是____(填“分子”或“原子”)
【答案】2:1:1:1 CO2、H2O 4个原子 原子
【解析】
A物质是氨气,化学式是NH3;B物质是二氧化碳,化学式是CO2;C物质是尿素,化学式是CO(NH2)2;D物质是水,化学式是H2O。
(1)根据图示可知,反应物是氨气和二氧化碳,在一定条件下反应,生成尿素和水。根据化学反应中的质量守恒定律的内容,化学反应前后,原子的个数不变,可配平该化学反应的化学反应方程式为: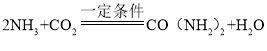 ,化学反应中,参加化学反应的分子的个数比等于化学方程式中各个物质分子的化学计量数之比。故答案为:2:1:1:1;
,化学反应中,参加化学反应的分子的个数比等于化学方程式中各个物质分子的化学计量数之比。故答案为:2:1:1:1;
(2)氧化物的定义是由两种元素组成,其中一种元素为氧元素的化合物叫做氧化物。符合该定义的只有B、D两种物质,即二氧化碳和水。故答案为:CO2、H2O;
(3)甲物质是氨气,氨气是由氨分子构成的,一个氨分子中,有一个氮原子,三个氢原子,即一个氨分子中有4个原子。故答案为:4个原子;
(4)化学反应中,分子可以再分,而原子不能再分。故不发生改变的微粒是原子。故答案为:原子。

 智慧小复习系列答案
智慧小复习系列答案【题目】某化学学习小组在完成“利用氯化钡溶液鉴别氯化钠和碳酸钠”的实验后,对废液缸中溶液的溶质成分进行了探究。请完成以下探究过程。
(提出问题)_____________?
(作出猜想)Ⅰ.溶质仅为氯化钠;Ⅱ溶质为氯化钡和氯化钠;Ⅲ._______________。
(设计方案)
实验操作 | 现象 | 结论 |
取少量废液缸中上层清液,向其中加入一定量的______________溶液。(填化学式,限填一种) | 无明显现象 | 猜想Ⅰ正确 |
______ | 猜想Ⅱ正确 | |
有气泡产生 | 猜想Ⅲ正确 |
(交流反思)学习小组经过讨论认为,含有可溶性钡盐的废液可以用碳酸钠溶液进行无害化处理。请写出硝酸钡与碳酸钠反应的化学方程式___________________。
若是人误吃了可溶性钡盐,不能服用碳酸钠溶液解毒而是服用硫酸钠溶液,理由是_______。
【题目】为测定镁和硫酸镁固体混合物中镁元素的质量分数,先称取5g混合物,放入一干净的烧杯中,然后取50g某溶质质量分数的稀硫酸,平均分五次加入其中,充分反应,实验所得数据如下表:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀硫酸的质量/g | 10 | 10 | 10 | 10 | 10 |
生成气体的总质量/g | 0.05 | m | 0.15 | 0.18 | n |
(l)上表中m=_____、n=_____.
(2)请计算所用稀硫酸的溶质质量分数(结果保留一位小数).____
(3)固体混合物中,硫酸镁的质量分数为_____.