题目内容
某研究性学习小组对碳粉与氧化铁反应的气体产物成分进行研究.
【提出假设】该反应的气体产物可能是CO2、或CO、或CO2和CO的混合物.
【查阅资料】氮气不与碳、氧化铁发生反应.
【实验方案】设计如图所示装置,将一定量的氧化铁和炭粉在隔绝空气的条件下充分反应,来测定反应后的气体成分.
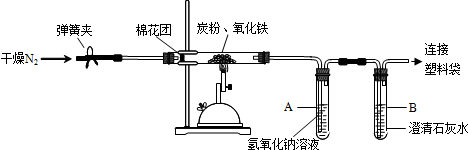
【实验操作步骤】
①加热,使反应物充分反应.
②冷却至室温,称得固体质量为50.24g、A增重0.88g.
③通一段时间纯净干燥的氮气,停止通入氮气后,夹紧弹簧夹.
④按上图连接装置,并检查装置的气密性.
⑤反应结束时停止加热,再缓缓通入一段时间的氮气.
⑥称取51.68g氧化铁和炭粉混合物,放入硬质玻璃管中.
【交流讨论】
(1)写出操作步骤的正确排序 .
(2)步骤③通入N2的目的是 ;B中澄清石灰水的作用是 .
(3)A中发生的反应的化学方程式为 .
(4)可以判定反应结束的实验现象是 .
(5)通过实验分析,该反应的气体产物是 ,其依据是 .
(6)检验反应后的固体中炭粉是否有剩余的实验步骤是:①取少量反应后的固体样品放入小烧杯;②向其中加入足量的 ;③观察到 ;④固体中含有剩余的炭粉.
(7)硬质玻璃管中发生氧化反应的物质是 _ .
【提出假设】该反应的气体产物可能是CO2、或CO、或CO2和CO的混合物.
【查阅资料】氮气不与碳、氧化铁发生反应.
【实验方案】设计如图所示装置,将一定量的氧化铁和炭粉在隔绝空气的条件下充分反应,来测定反应后的气体成分.

【实验操作步骤】
①加热,使反应物充分反应.
②冷却至室温,称得固体质量为50.24g、A增重0.88g.
③通一段时间纯净干燥的氮气,停止通入氮气后,夹紧弹簧夹.
④按上图连接装置,并检查装置的气密性.
⑤反应结束时停止加热,再缓缓通入一段时间的氮气.
⑥称取51.68g氧化铁和炭粉混合物,放入硬质玻璃管中.
【交流讨论】
(1)写出操作步骤的正确排序
(2)步骤③通入N2的目的是
(3)A中发生的反应的化学方程式为
(4)可以判定反应结束的实验现象是
(5)通过实验分析,该反应的气体产物是
(6)检验反应后的固体中炭粉是否有剩余的实验步骤是:①取少量反应后的固体样品放入小烧杯;②向其中加入足量的
(7)硬质玻璃管中发生氧化反应的物质是
考点:实验探究物质的组成成分以及含量,常见气体的检验与除杂方法,碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【交流讨论】
(1)熟悉实验操作步骤;
(2)通入N2的目的是排尽空气;澄清石灰水可检验二氧化碳的存在;
(3)氢氧化钠溶液可吸收二氧化碳,生成碳酸钠和水;
(4)气体不再产生就是实验结束;
(5)从如果全部是二氧化碳,减少的反应物质量应等于A中增重(CO2的质量)考虑;
(6)根据炭粉不与酸反应,而炭与氧化铁反应的固体产物铁能与酸反应判断;
(7)碳和一氧化碳都能与氧化铁发生反应.
(1)熟悉实验操作步骤;
(2)通入N2的目的是排尽空气;澄清石灰水可检验二氧化碳的存在;
(3)氢氧化钠溶液可吸收二氧化碳,生成碳酸钠和水;
(4)气体不再产生就是实验结束;
(5)从如果全部是二氧化碳,减少的反应物质量应等于A中增重(CO2的质量)考虑;
(6)根据炭粉不与酸反应,而炭与氧化铁反应的固体产物铁能与酸反应判断;
(7)碳和一氧化碳都能与氧化铁发生反应.
解答:解:(1)实验操作步骤的正确排序是:④⑥③①⑤②;
(2)氮气不与碳、氧化铁发生反应.而空气中的一些气体却能反应,所以通入氮气的目的是排尽空气;B中澄清石灰水的作用是检验A是否将二氧化碳是否吸收完全.
故答案为:排尽空气;检验A是否将二氧化碳是否吸收完全;
(3)A中发生的反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O;
故答案为:CO2+2NaOH═Na2CO3+H2O;
(4)气体不再产生就是实验结束,即试管A和B中均无气泡产生;
故答案为:试管A和B中均无气泡产生;
(5)如果全部是二氧化碳,减少的反应物质量应等于A中增重(CO2的质量),但减少的反应物质量多于A中增重(CO2的质量),说明该反应的气体产物是CO2和CO的混合物.
故答案为:CO2和CO的混合物;减少的反应物质量多于A中增重(CO2的质量);
(6)若要检验反应后的固体中炭粉是否有剩余,可向烧杯中加入足量的稀盐酸或稀硫酸,炭粉不与酸反应,而炭与氧化铁反应的固体产物铁能与酸反应.烧杯底部有不溶解的黑色固体,说明固体中含有剩余的炭粉.
故答案为:向烧杯中加入足量的稀盐酸或稀硫酸;烧杯底部有不溶解的黑色固体;
(7)高温下,碳和一氧化碳都能与氧化铁发生反应,由(5)知,该实验反应的气体产物是CO2和CO的混合物,所以硬质玻璃管中发生氧化反应的物质是碳和一氧化碳;故答案为:炭粉;一氧化碳.
故本题答案为:
(1)④⑥③①⑤②;
(2)排尽空气;检验A是否将二氧化碳是否吸收完全;
(3)CO2+2NaOH═Na2CO3+H2O;
(4)试管A和B中均无气泡产生;
(5)CO2和CO的混合物;减少的反应物质量多于A中增重(CO2的质量);
(6)向烧杯中加入足量的稀盐酸或稀硫酸;烧杯底部有不溶解的黑色固体;
(7)炭粉;一氧化碳.
(2)氮气不与碳、氧化铁发生反应.而空气中的一些气体却能反应,所以通入氮气的目的是排尽空气;B中澄清石灰水的作用是检验A是否将二氧化碳是否吸收完全.
故答案为:排尽空气;检验A是否将二氧化碳是否吸收完全;
(3)A中发生的反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O;
故答案为:CO2+2NaOH═Na2CO3+H2O;
(4)气体不再产生就是实验结束,即试管A和B中均无气泡产生;
故答案为:试管A和B中均无气泡产生;
(5)如果全部是二氧化碳,减少的反应物质量应等于A中增重(CO2的质量),但减少的反应物质量多于A中增重(CO2的质量),说明该反应的气体产物是CO2和CO的混合物.
故答案为:CO2和CO的混合物;减少的反应物质量多于A中增重(CO2的质量);
(6)若要检验反应后的固体中炭粉是否有剩余,可向烧杯中加入足量的稀盐酸或稀硫酸,炭粉不与酸反应,而炭与氧化铁反应的固体产物铁能与酸反应.烧杯底部有不溶解的黑色固体,说明固体中含有剩余的炭粉.
故答案为:向烧杯中加入足量的稀盐酸或稀硫酸;烧杯底部有不溶解的黑色固体;
(7)高温下,碳和一氧化碳都能与氧化铁发生反应,由(5)知,该实验反应的气体产物是CO2和CO的混合物,所以硬质玻璃管中发生氧化反应的物质是碳和一氧化碳;故答案为:炭粉;一氧化碳.
故本题答案为:
(1)④⑥③①⑤②;
(2)排尽空气;检验A是否将二氧化碳是否吸收完全;
(3)CO2+2NaOH═Na2CO3+H2O;
(4)试管A和B中均无气泡产生;
(5)CO2和CO的混合物;减少的反应物质量多于A中增重(CO2的质量);
(6)向烧杯中加入足量的稀盐酸或稀硫酸;烧杯底部有不溶解的黑色固体;
(7)炭粉;一氧化碳.
点评:典型的实验分析题,综合性强,难度大,只有熟练掌握所学物质的性质和基本实验操作步骤才能准确得到答案.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 实验室中有一瓶标签受损的无色液体,如图所示.这瓶无色液体是什么呢?实验室老师告诉大家,该液体目前只能是过氧化氢溶液和蒸馏水中的一种.
实验室中有一瓶标签受损的无色液体,如图所示.这瓶无色液体是什么呢?实验室老师告诉大家,该液体目前只能是过氧化氢溶液和蒸馏水中的一种. 如图所示是甲、乙、丙三种物质的溶解度曲线,在20℃时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题:
如图所示是甲、乙、丙三种物质的溶解度曲线,在20℃时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题: