题目内容
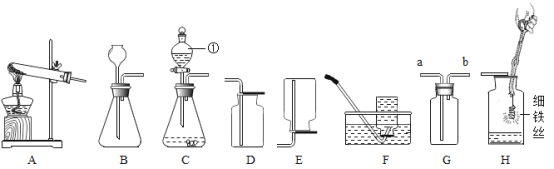
【题目】老师用如图所示装置为同学们做了一个实验。A装置中盛有二氧化锰黑色粉末,B装置中盛有足量的澄清石灰水,C装置中盛有足量的稀盐酸,气球中装有少量的碳酸钙粉末。
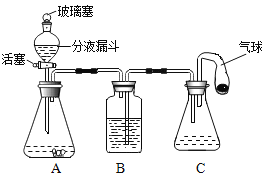
(1)打开分液漏斗的活塞和玻璃塞,使A装置与大气相通,将气球中的碳酸钙粉末全部倒入稀盐酸中,可以观察到C装置中的现象是________________,发生反应的化学方程式为___________________ 。
(2)待上述反应结束后,从分液漏斗注入足量的过氧化氢溶液,关闭活塞和玻璃塞,A装置中发生反应的化学方程式为___________________。
(3)在整个实验过程中,B装置中的现象是 _______________________。
(4)C装置中气球的作用是______________(填字母)。
A收集纯净气体 B添加固体药品
C调节C装置容积 D控制气体总量
【答案】有无色气泡逸出,白色固体消失,气球微微鼓起 CaCO3+2HCl=CaCl2+CO2↑+H2O 2H2O2![]() 2H2O+O2↑ 澄清石灰水先变浑浊,后来浊液被压入C中,液面下降 BC
2H2O+O2↑ 澄清石灰水先变浑浊,后来浊液被压入C中,液面下降 BC
【解析】
(1)碳酸钙与稀盐酸反应,固体物质渐渐溶解同时放出气体.碳酸钙与稀盐酸反应生成氯化钙、二氧化碳和水。
故答:有无色气泡逸出,白色固体消失,气球微微鼓起;
![]()
(2)在二氧化锰催化下,过氧化氢分解生成水和氧气,方程式为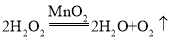
(3)整个过程中,先是C中产生的二氧化碳通入B装置,石灰水变浑浊; 接下来,A装置中产生的氧气进入B瓶,而使瓶内压强增大,装置B中浊液被排入C装置.
故答:澄清石灰水先变浑浊,后来浊液被压入C中,液面下降.
(4)实验前气球内放有碳酸钙固体,所以气球此时的作用为添加药品; 待装置B中浊液流入C装置,碳酸钙与盐酸反应放出气体二氧化碳,此时气球起到容器的作用.
故选BC.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】乙醇不完全燃烧时产生CO、CO2和H2O。依据下表数据分析得出的结论中,不正确的是:
物质 | 乙醇 | 氧气 | 二氧化碳 | 水 | 一氧化碳 |
反应前质量/g | 6.6 | 8.8 | 0 | 0 | 0 |
反应后质量/g | 2 | 0 | 6.6 | 5.4 | a |
A. 表中的a值为1.4 B. 在化学反应前后碳元素质量一定相等
C. 参加反应的乙醇和氧气的质量比为3:4 D. 生成的CO和CO2分子个数比为1:3