题目内容
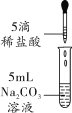
【题目】在学习了盐的化学性质后,同学们在课外小组活动时做了碳酸钠溶液与稀盐酸反应的实验(如图)。实验中没有观察到有气泡产生,该反应所得无色液体中的溶质有哪些成分呢?同学们对此进行了以下探究:
(查阅资料)①碳酸钠和稀盐酸反应不仅可以生成二氧化碳,还可以生成碳酸氢钠。
②碳酸氢钠与氯化钙溶液混合不发生反应;而碳酸钠溶液与氯化钙溶液反应生成沉淀。
(提出问题)实验所得溶液中是否含有碳酸氢钠?
(进行实验)实验一:取所得溶液于试管中,加入足量的____(写化学式)溶液,观察到______。
实验二:静置,取上层清液,滴加适量____,观察到_____,证明所得溶液中含有碳酸氢钠。
(反思讨论)(1)实验一中,所加足量溶液的目的是_____。
(2)写出实验二所发生反应的化学方程式_____。
(拓展延伸)联想到课本中所学的碳酸钠与稀盐酸反应生成二氧化碳,同学们做了对比实验(如图),结果观察到有气泡产生。对比分析后,大家认为,当反应物的量不同时,产物可能不同。试另举一例:____。
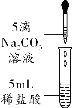
【答案】CaCl2 产生白色沉淀 稀盐酸 产生气泡 彻底除去溶液中的碳酸钠,以免对碳酸氢钠的检验造成干扰 NaHCO3+HCl=NaCl+H2O+ CO2↑ 氧气足量时,碳燃烧生成二氧化碳,氧气不足时,碳燃烧生成一氧化碳(合理即可)
【解析】
【进行实验】实验一:所得溶液中一定含有碳酸钠,加入氯化钙溶液,碳酸钠与氯化钙反应生成碳酸钙白色沉淀和氯化钠。实验二:碳酸氢钠与稀盐酸反应产生二氧化碳,为检验是否含有碳酸氢钠,需在上层清液中滴加稀盐酸,观察是否产生气泡。【反思讨论】(1)碳酸钠、碳酸氢钠均能与稀盐酸反应生成二氧化碳,为检验是否含有碳酸氢钠,需排除碳酸钠的干扰,因此加入足量氯化钙溶液的目的是彻底除去溶液中的碳酸钠,防止其对碳酸氢钠的检验造成干扰。(2)碳酸氢钠与稀盐酸反应生成氯化钠、水和二氧化碳。【拓展延伸】当反应物的量不同时,产物可能不同,例如氧气足量时,碳燃烧生成二氧化碳,氧气不足时,碳燃烧生成一氧化碳等。

 阅读快车系列答案
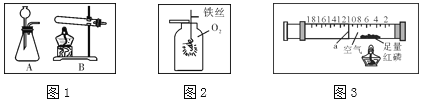
阅读快车系列答案【题目】小杰同学在复习铁生锈条件时知道,常温下,没有氧气,铁与水几乎不反应。老师告诉同学们,高温下,铁与水蒸气能反应生成一种常见的铁的氧化物和一种气体。小杰很好奇,设计如图所示实验探究铁粉与水蒸气反应后的产物。
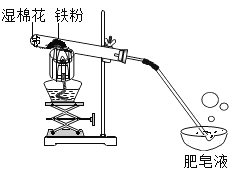
(1)试管尾部放一团湿棉花的目的是___________________。
(2)探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是_________________。
(3)探究试管中剩余固体成分是什么?
(查阅资料)常见的铁的氧化物有FeO(黑色、没有磁性)、![]() 、
、![]() 。
。
(初步验证)试管中固体为黑色,能全部被磁铁吸引。
(猜想与假设)猜想一:剩余固体是![]() ;猜想二剩余固体是__________________。
;猜想二剩余固体是__________________。
(实验探究)
实验操作 | 实验现象结论 |
______________________ | ___________________证明猜想一正确 |
(实验结论)铁和水蒸气反应的化学方程式:___________________。
(反思与交流)该黑色固体不可能是![]() ,理由是___________________。
,理由是___________________。
【题目】(2017雅安)馒头、面包等发面食品的一个特点是面团中有许多小孔,他们使发面食品松软可口。小明学习相关化学知识后,将家里制作馒头用的白色粉末带到实验室与兴趣小组的同学一起进行探究。
(初步探究)取少量白色粉末于试管中,加适量水,测得溶液的pH>7,说明溶液呈________性。
(提出问题)白色粉末成分是什么?
(查阅资料)
(1)碳酸钠、碳酸氢钠都可用于制作发面食品。
(2)碳酸氢钠不稳定,受热易分解生成二氧化碳和水等; 碳酸钠很稳定。
(猜想与假设)
猜想Ⅰ:碳酸钠
猜想Ⅱ:碳酸氢钠
(实验探究)甲乙兴趣小组设计不同实验方案进行探究。
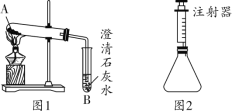
甲组方案:如图,取适量白色粉末于试管中,将导管伸入澄清石灰水,加热,澄清石灰水变浑浊,猜想Ⅱ正确。写出装置B中反应的化学方程式____________。
乙组方案:用如图所示装置作为反应容器,准确测量生成气体的体积以判断白色粉末的成分。
分别向盛有碳酸钠、碳酸氢钠和白色粉末的锥形瓶中,注入等体积、等浓度的足量的稀盐酸,记录如表:
实验编号 | 锥形瓶内物质 | 最终得到CO2体积 /mL | |
名称 | 质量/g | ||
① | 碳酸钠 | a | V1 |
② | 碳酸氢钠 | a | V2 |
③ | 白色粉末 | m | V3 |
实验①的化学反应方程式为______________;表中m=________g;根据上表中数据分析,猜想Ⅱ正确,判断的依据是______________。
(反思应用)
(1)甲组方案中,无法判断白色粉末是否为碳酸钠和碳酸氢钠的混合物;乙组方案可以判断,如果是两者的混合物,应该满足的条件是__________________。
(2)家中制作馒头、面包时,将面粉发酵(产生有机酸),再加入适量的碳酸氢钠,可以使馒头、面包松软。原因是________________。
【题目】常温下,往盛放适量M物质的烧杯中逐渐加入N物质并充分搅拌。右下图横坐标x表示N物质的质量,纵坐标y表示烧杯中的某物理量(见下表)。下列实验与图像对应关系合理的是
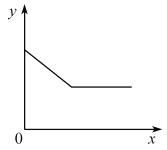
M | N | y | |
A | 水 | 氧化钙 | 溶液的温度 |
B | 水 | 氢氧化钠 | 溶液的pH |
C | 饱和氯化钠溶液 | 氯化钠 | 溶液的溶质质量分数 |
D | 硫酸铜溶液 | 铁粉 | 溶液的质量 |