题目内容
点燃的镁条能在二氧化碳中继续燃烧,且燃烧时产生大量黑烟,还生成一种白反固体.则燃烧过程中发生的化学方程式为 ,该反应中还原剂是 ;根据化学方程式能获得信息: ; ; (答三条).
【答案】分析:由题目中所给”镁在CO2中燃烧产生黑烟,并有白色固体产生”可知镁与二氧化碳反应生成黑烟是碳,白色固体是氧化镁.在化合价有改变的氧化还原反应中,化合价由低变高的物质称作还原剂.根据化学方程式的含义判断,化学方程式的含义主要有四点:①表示反应物,②表示生成物,③表示反应条件,④反映各物质间量的关系,由此得到的信息更多,如生成物的状态,物质的结构和组成等.
解答:解:根据题干中信息可知:镁与二氧化碳 在点燃条件下,生成了氧化镁和碳.所以化学方程式可以表示为:2Mg+CO2 2MgO+C;其中化合价升高的物质是还原剂 Mg由0价变为+2价,所以该反应中作还原剂的是 Mg.故此化学方程式可表示反应物为镁和二氧化碳,生成物为氧化镁和碳,反应条件为点燃.
2MgO+C;其中化合价升高的物质是还原剂 Mg由0价变为+2价,所以该反应中作还原剂的是 Mg.故此化学方程式可表示反应物为镁和二氧化碳,生成物为氧化镁和碳,反应条件为点燃.
故答案为:2Mg+CO2 2MgO+C;Mg;反应物为镁和二氧化碳;生成物为氧化镁和碳;反应条件为点燃;
2MgO+C;Mg;反应物为镁和二氧化碳;生成物为氧化镁和碳;反应条件为点燃;
点评:本题考查如何正确书写化学方程式,首先要熟记遵循的基本原则;然后才能够正确写出化学方程式,对与给予信息的题目,首先要找出它的反应物和生成物是什么,反应条件.对于还原剂在初中是难点,也不是常考知识点,一定意义上有点超出初中所学范围活.常见还原剂是活泼的金属单质,如Na,Al,Zn,Fe等.和某些非金属单质,如H2,C,Si等.元素(如C,S等)处于低化合价.
解答:解:根据题干中信息可知:镁与二氧化碳 在点燃条件下,生成了氧化镁和碳.所以化学方程式可以表示为:2Mg+CO2
 2MgO+C;其中化合价升高的物质是还原剂 Mg由0价变为+2价,所以该反应中作还原剂的是 Mg.故此化学方程式可表示反应物为镁和二氧化碳,生成物为氧化镁和碳,反应条件为点燃.
2MgO+C;其中化合价升高的物质是还原剂 Mg由0价变为+2价,所以该反应中作还原剂的是 Mg.故此化学方程式可表示反应物为镁和二氧化碳,生成物为氧化镁和碳,反应条件为点燃.故答案为:2Mg+CO2
 2MgO+C;Mg;反应物为镁和二氧化碳;生成物为氧化镁和碳;反应条件为点燃;
2MgO+C;Mg;反应物为镁和二氧化碳;生成物为氧化镁和碳;反应条件为点燃;点评:本题考查如何正确书写化学方程式,首先要熟记遵循的基本原则;然后才能够正确写出化学方程式,对与给予信息的题目,首先要找出它的反应物和生成物是什么,反应条件.对于还原剂在初中是难点,也不是常考知识点,一定意义上有点超出初中所学范围活.常见还原剂是活泼的金属单质,如Na,Al,Zn,Fe等.和某些非金属单质,如H2,C,Si等.元素(如C,S等)处于低化合价.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
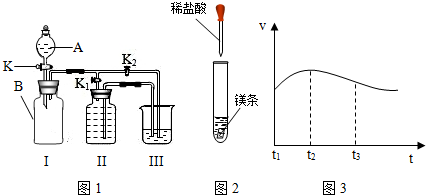
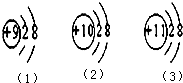 回答下列问题:
回答下列问题:
 分类标准有多种,请自拟两个分类标准,将水(H2O)、氧气(O2)、二氧化碳(CO2)、甲烷(CH4)四种物质中的三种包括在一种标准内,而另一种不包括在标准内。
分类标准有多种,请自拟两个分类标准,将水(H2O)、氧气(O2)、二氧化碳(CO2)、甲烷(CH4)四种物质中的三种包括在一种标准内,而另一种不包括在标准内。 列三种微粒的结构,找出相同点和不同点。(2分)
列三种微粒的结构,找出相同点和不同点。(2分)
 分类标准有多种,请自拟两个分类标准,将水(H2O)、氧气(O2)、二氧化碳(CO2)、甲烷(CH4)四种物质中的三种包括在一种标准内,而另一种不包括在标准内。
分类标准有多种,请自拟两个分类标准,将水(H2O)、氧气(O2)、二氧化碳(CO2)、甲烷(CH4)四种物质中的三种包括在一种标准内,而另一种不包括在标准内。 列三种微粒的结构,找出相同点和不同点。(2分)
列三种微粒的结构,找出相同点和不同点。(2分)