题目内容
(2012?曲阜市模拟)以电解食盐水为基础制取氯气、氢氧化钠等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一.由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不符合电解要求,因此必须经过精制.以粗盐为原料的“氯碱工业”流程如下:
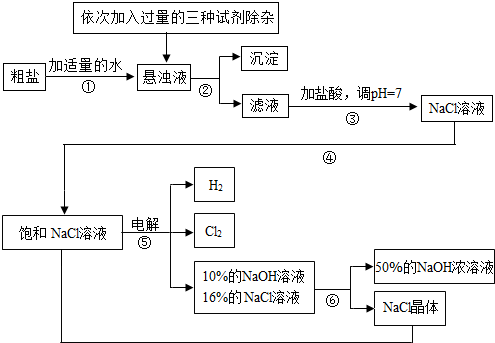
回答下列问题:
(1)操作④的名称是
(2)操作①②间除杂质时所加的三种试剂是NaOH溶液、Na2CO3溶液、BaCl2溶液(均过量),其顺序要求是:Na2CO3,溶液必须在BaCl2溶液之
(3)电解饱和NaCl溶液的化学方程式是

回答下列问题:
(1)操作④的名称是
蒸发
蒸发
.(2)操作①②间除杂质时所加的三种试剂是NaOH溶液、Na2CO3溶液、BaCl2溶液(均过量),其顺序要求是:Na2CO3,溶液必须在BaCl2溶液之
后
后
(填“前”或“后”)加入,原因是Na2CO3可以与过量的BaCl2反应,转变成NaCl和BaCO3沉淀
Na2CO3可以与过量的BaCl2反应,转变成NaCl和BaCO3沉淀
,有同学提出用Ba(OH)2
Ba(OH)2
溶液代替BaCl2溶液可达到同样的目的.(3)电解饱和NaCl溶液的化学方程式是
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
.
| ||
分析:根据题干提供的信息结合物质的性质进行分析,要将氯化钠溶液变成氯化钠的饱和溶液,可以采用加热蒸发的方法;在除去氯化钠中混有的可溶性杂质时,所加入的试剂反应后不能引入新的杂质,后面加的试剂要能把前面加的多余的试剂除掉,据此解答即可.
解答:解:(1)氯化钠溶液经过操作④得到了氯化钠的饱和溶液,则该操作是蒸发,故填:蒸发;
(2)Na2CO3,溶液必须在BaCl2溶液之后,以便把多余的氯化钡溶液反应掉,防止含有新的杂质,要除去硫酸根离子,还可以使用氢氧化钡溶液,反应后能生成硫酸钡沉淀和氢氧化钠,生成的氢氧化钠能在后面加入盐酸时反应生成氯化钠,故填:后,Na2CO3可以与过量的BaCl2反应,转变成NaCl和BaCO3沉淀,Ba(OH)2;
(3)电解饱和氯化钠溶液,能生成氢氧化钠、氯气和氢气,故填:2NaCl+2H2O
2NaOH+H2↑+Cl2↑.
(2)Na2CO3,溶液必须在BaCl2溶液之后,以便把多余的氯化钡溶液反应掉,防止含有新的杂质,要除去硫酸根离子,还可以使用氢氧化钡溶液,反应后能生成硫酸钡沉淀和氢氧化钠,生成的氢氧化钠能在后面加入盐酸时反应生成氯化钠,故填:后,Na2CO3可以与过量的BaCl2反应,转变成NaCl和BaCO3沉淀,Ba(OH)2;
(3)电解饱和氯化钠溶液,能生成氢氧化钠、氯气和氢气,故填:2NaCl+2H2O
| ||
点评:本题考查了常见物质间的转化,完成此题,可以依据已有的物质的性质进行.书写反应的化学方程式要注意配平.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 (2012?曲阜市模拟)实验室有一瓶未知浓度的BaCl2溶液,某同学取出150g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液.反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图甲所示.请计算:
(2012?曲阜市模拟)实验室有一瓶未知浓度的BaCl2溶液,某同学取出150g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液.反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图甲所示.请计算: