题目内容
(2012?惠安县质检)在矿山、坑道等缺氧的场合,工人们往往可利用自己呼出的二氧化碳与过氧化钠粉末(Na2O2)作用获得所需要的氧气,并处理呼出的二氧化碳.某工人在一次坑道作业中预计消耗氧气800g,则他至少准备多少克过氧化钠?(有关反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2)
分析:根据反应方程式为2Na2O2+2CO2=2Na2CO3+O2,将需要的氧气的质量代入化学反应方程式即可计算理论上需要的过氧化钠的质量.
解答:解:设消耗氧气800g,则他至少准备过氧化钠的质量是x
则2Na2O2+2CO2=2Na2CO3+O2,
2×78 32
x 800g
=
解得x=3900g,
答:至少准备3900克过氧化钠.
则2Na2O2+2CO2=2Na2CO3+O2,
2×78 32
x 800g
| 2×78 |
| x |
| 32 |
| 800g |
解得x=3900g,
答:至少准备3900克过氧化钠.
点评:本题考查学生利用化学反应方程式的计算,学生应注意利用发生的反应将某物质的质量代入计算,应注意解答格式的规范.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

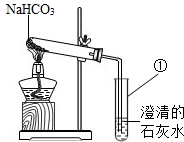 (2012?惠安县质检)【探究实验1】碳酸氢钠溶液的酸碱性.
(2012?惠安县质检)【探究实验1】碳酸氢钠溶液的酸碱性.