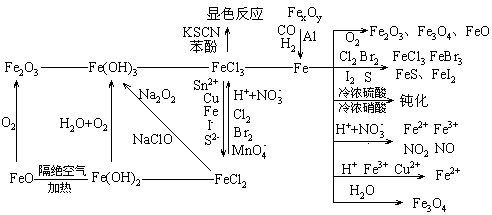
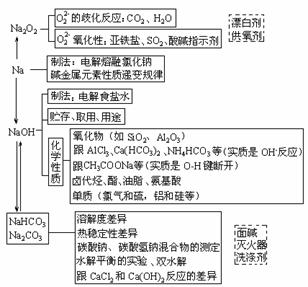
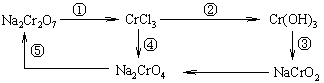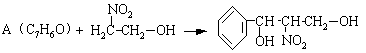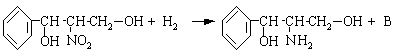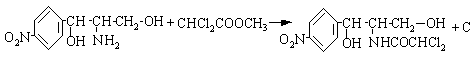1.金属的通性
金属的化学性质主要表现为易失去最外层的电子,显示还原性,这与它们的原子结构有关。常见金属的主要化学性质列于下表:
|
金属活动性 顺序 |
K Ca Na Mg Al Mn Zn Fe Sn Pb (H)Cu Hg Ag Pt Au |
||||
|
金属原子 失电子能力 |
 依次减小,还原性减弱
依次减小,还原性减弱 |
||||
|
空气中跟氧气的反应 |
易被氧化 |
常温时能被氧化 |
|
加热时能被氧化 |
不能被氧化 |
|
跟水的反应 |
常温可置换出水中的氢 |
加热或与水蒸气反应时能置换出水中的氢 |
|
不与水反应 |
|
|
跟酸的反应 |
能置换出稀酸(如HCl、H2SO4)中的氢 |
|
不能置换出稀酸中的氢 |
||
|
反应剧烈 |
反应程度依次减弱 |
|
能跟浓硫酸、硝酸反应 |
能跟王水反应 |
|
|
跟盐的反应 |
位于金属活动性顺序前面的金属可以将后面的金属从其盐溶液中置换出来 |
||||
|
跟碱的反应 |
Al、Zn等具有两性的金属可以与碱反应 |