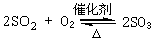8. (09四川卷26)(16分)
过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
Ⅰ.测定过氧化的含量
请填写下列空白:
(1)
移取10.00
m密度为ρ g/mL的过氧化氢溶液至250mL ___________(填仪器名称)中,加水衡释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样
(2) 用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。
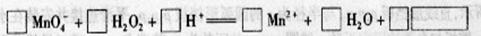
(3) 滴定时,将高锰酸钾标准溶液注入______________________(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是___________________________________________
______________________________________________________________。
(4) 复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为______________________________________。
(5) 若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________(填“偏高”或“偏低”或“不变”)。
Ⅱ.探究过氧化氢的性质
该化学举小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾演粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)
请将他们的实验方法和实验现象填入下表:
|
实 验 内 容 |
实 验 方 法 |
实 验 现 象 |
|
验证氧化性 |
|
|
|
验证不稳定性 |
|
|
答案:
I.(1)容量瓶
(2)2 5 6 2 8 502
(3)酸式
滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色
(4)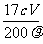
(5)偏高
II.(各1分,共4分)
|
实验内容 |
实验方法 |
实验现象 |
|
验证氧化性 |
取适量饱和硫化氢溶液于试管中,滴入 过氧化氢溶液。 (取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液。) |
产生淡黄色沉淀或溶液变浑浊。 (溶液变蓝色。) |
|
验证不稳定性 |
取适量过氧化氢溶液于试管中,加热, 用带火星的木条检验。 (取适量过氧化氢溶液于试管中,加热,用导气管将得到的气体通入到装有饱和硫化氢溶液的试管中。) |
产生气泡,木条复燃。 (溶液变浑浊或有浅黄色沉淀产生) |
7. (09全国卷Ⅰ27)(15分)
浓H2SO4和木炭在加热时发生反应的化学方程式是
2 H2SO4 (浓) + C  CO2↑+ 2 H2O + 2SO2↑
CO2↑+ 2 H2O + 2SO2↑
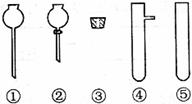
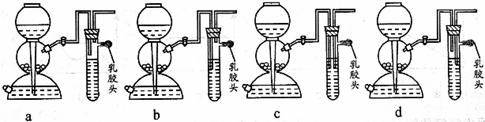
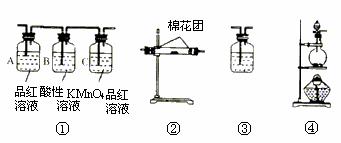
请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)
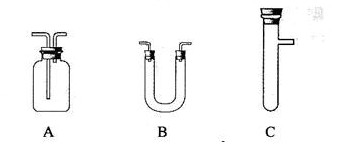
 将所选的仪器按连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。
将所选的仪器按连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。
|
选用的仪器 (填字母) |
加入的试剂 |
作用 |
|
|
|
|
答案:
C 浓硫硫和木炭 产生反应物
B 无水硫酸铜 检验是否有水
A 品红 检验SO2
A 酸性KMnO4 除去SO2
A 澄清石灰水 检验CO2的存在。
解析: 成套装置包括反应装置,检验装置和尾气处理装置。C中加入浓硫硫和木炭作为反应物的发生器,产物中必须先检验水,因为在检验其他物质时会在其它试剂中混入水,可选用装置B,放入无水硫酸铜,若变蓝则说明有水。接着检验SO2气体,用装置A,放入品红检验,若品红褪色,则说明有SO2气体产生,再用装置A,放入酸性KMnO4溶液以除去SO2,最后再用装置A,放入澄清石灰水来检验CO2的存在,因SO2也可以使澄清石灰水变浑,故先要除去SO2。
成套装置包括反应装置,检验装置和尾气处理装置。C中加入浓硫硫和木炭作为反应物的发生器,产物中必须先检验水,因为在检验其他物质时会在其它试剂中混入水,可选用装置B,放入无水硫酸铜,若变蓝则说明有水。接着检验SO2气体,用装置A,放入品红检验,若品红褪色,则说明有SO2气体产生,再用装置A,放入酸性KMnO4溶液以除去SO2,最后再用装置A,放入澄清石灰水来检验CO2的存在,因SO2也可以使澄清石灰水变浑,故先要除去SO2。
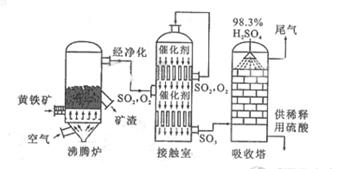
1.生产过程:
|
三阶段 |
SO2制取和净化 |
SO2转化为SO3 |
SO3吸收和H2SO4的生成 |
|
三方程 |
4FeS2(s)+11O2(g) = 2Fe2O3(s)+8SO2(g); △H=-3412 kJ/mol |
2SO2(g)+O2(g)  2SO3(g); 2SO3(g);△H=-196.6 kJ/mol |
SO3(g)+H2O(l)=H2SO4(l);△H=-130.3 kJ/mol |
|
三设备 |
沸腾炉 |
接触室 |
吸收塔 |
|
有 关 原 理 |
矿石粉碎,以增大矿石与空气的接触面,加快反应速率 |
逆流原理(热交换器)目的: 冷热气体流向相反,冷的SO2、O2、N2被预热,而热的SO3、SO2、O2、N2被冷却 |
逆流原理(98.3%的浓硫酸从塔顶淋下,气体由下往上,流向相反,充分接触,吸收更完全) |
|
设备中排出的气 体 |
炉气:SO2.N2.O2.矿尘(除尘).砷硒化合物(洗涤). H2O气(干燥)…… 净化气:SO2.N2.O2 |
SO2、O2、N2、SO3 |
尾气:SO2及N2、O2 不能直接排入大气中 |
|
说 明 |
矿尘.杂质:易使催化剂“中毒” H2O气:腐蚀设备、影响生产 |
反应条件-- 理论需要:低温、高压、催化剂;实际应用:400℃-500℃、常压、催化剂  |
实际用98.3%的浓硫酸吸收SO3,以免形成酸雾不利于气体三氧化硫被进一步吸收 |
 变大
变大
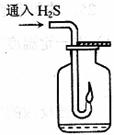
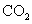 通入
通入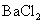 溶液中至饱和,无沉淀产生;再通入
溶液中至饱和,无沉淀产生;再通入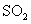 ,产生沉淀
,产生沉淀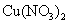 固体,铜粉仍不溶解
固体,铜粉仍不溶解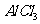 溶液中滴加氨水,产生白色沉淀;再加入
溶液中滴加氨水,产生白色沉淀;再加入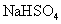 溶液,沉淀消失
溶液,沉淀消失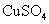 固体,速率不改变
固体,速率不改变 SO3+NO ②SO3+H2O
SO3+NO ②SO3+H2O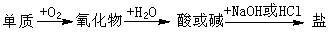

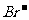 B.
B.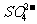 C.
C.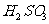 D.
D. 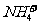
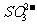 被氧化得到硫酸根。所以不能确定是否有硫酸根离子。
被氧化得到硫酸根。所以不能确定是否有硫酸根离子。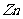 与
与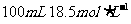 的浓
的浓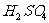 充分反应,
充分反应,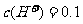
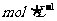 。则气体A中各组分的体积比为
。则气体A中各组分的体积比为 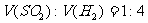
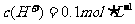 ,则
,则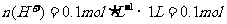 ,故反应后溶液中剩余硫酸0.05mol。由于浓硫酸与
,故反应后溶液中剩余硫酸0.05mol。由于浓硫酸与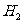 、
、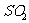 两种气体产生。设
两种气体产生。设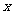 、
、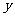
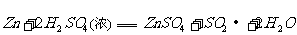
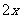
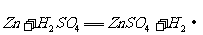
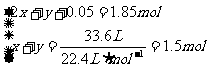
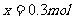
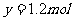
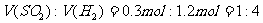

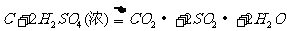
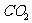
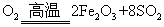
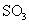 气体与
气体与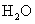 化合放出260.6kJ的热量,该反应的热化学方程是 。
化合放出260.6kJ的热量,该反应的热化学方程是 。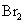 。
。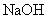 溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量
溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量