3.硫的氧化物
(1)二氧化硫:
①SO2是无色而有刺激性气味的有毒气体,密度比空气大,容易液化,易溶于水。
②SO2是酸性氧化物,能跟水反应生成亚硫酸,亚硫酸是中强酸。
③SO2有强还原性 常见氧化剂(见上)均可与SO2发生氧化一还原反应
如:SO2 + Cl 2 +2H2O == H2SO4 + 2HCl
④SO2也有一定的氧化性 2H2S + SO2 == 3S↓ +2H2O
⑤SO2具有漂白性,能跟有色有机化合物生成无色物质(可逆、非氧化还原反应)
⑥实验室制法:Na2SO3 + H2SO4(浓) == Na2SO3 + H2O +SO2↑
或Cu +
2H2SO4(浓) 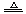 CuSO4 + 2H2O + SO2↑
CuSO4 + 2H2O + SO2↑
(2)三氧化硫:是一种没有颜色易挥发的晶体;具有酸性氧化物的通性,遇水剧烈反应生成硫酸并放出大量的热
(3)比较SO2与CO2、SO3
|
|
SO2 |
CO2 |
SO3 |
|
主要物性 |
无色、有刺激性气体、易液化易溶于水(1:40) |
无色、无气味气体能溶于水(1:1) |
无色固体.熔点(16.8℃) |
|
与水反应 |
 SO2+H2O H2SO3 中强酸 SO2+H2O H2SO3 中强酸 |
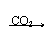 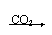  CO2+H2O H2CO3
弱酸 CO2+H2O H2CO3
弱酸 |
SO3+H2O==H2SO4(强酸) |
|
与碱反应 |
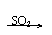 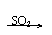 Ca(OH)2 CaSO3↓ Ca(HSO3)2 清液 白 清液 |
Ca(OH)2 CaCO3↓ Ca(HCO3)2 清液 白↓ 清液 |
SO3+Ca(OH)2==CaSO4(微溶) |
|
紫色石蕊 |
变红 |
变红 |
变红 |
|
品红 |
褪色 |
不褪色 |
不褪色 |
|
鉴定存在 |
能使品红褪色 又能使清石灰变浑浊 |
不能使品红褪色 但能使清石灰水变浑浊 |
|
|
氧化性 |
SO2+2H2S=2S↓+2H2O |
CO2+2Mg = 2MgO+C CO2+C = 2CO |
|
|
还原性 |
有 |
无 |
|
|
与Na2O2作用 |
Na2O2+SO2==Na2SO4 |
2Na2O2+2CO2==2Na2CO3+O2 |
2Na2O2+2SO3 ==2NaSO4+O2↑ |
1、氧族元素的原子结构及性质的递变规律
|
元素 |
氧(O) |
硫(S) |
硒(Se) |
碲(Te) |
|
核电荷数 |
8 |
16 |
34 |
52 |
|
最外层电子数 |
6 |
6 |
6 |
6 |
|
电子层数 |
2 |
3 |
4 |
5 |
|
化合价 |
-2 |
-2,+4,+6 |
-2,+4,+6 |
-2,+4,+6 |
|
原子半径 |
|
|||
|
密度 |
|
|||
|
与H2化合难易 |
点燃剧烈反应 |
加热时化合 |
较高温度时化合 |
不直接化合 |
|
氢化物稳定性 |
|
|||
|
氧化物化学式 |
-- |
SO2 SO3 |
SeO2 SeO3 |
TeO2 TeO3 |
|
氧化物对应水化物化学式 |
-- |
H2SO3 H2SO4 |
H2SeO3 H2SeO4 |
H2TeO3 H2TeO4 |
|
最高价氧化物水化物酸性 |
|
|||
|
元素非金属性 |
|
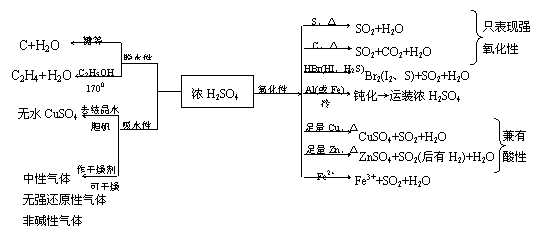
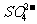 的鉴定(干扰离子可能有:
的鉴定(干扰离子可能有: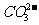 、
、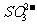 -、
-、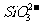 -、Ag+、
-、Ag+、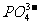 等):
等): 澄清液
澄清液 白色沉淀(说明待测液中含有SO42-离子)
白色沉淀(说明待测液中含有SO42-离子)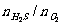 ≥2/1时,2H2S+O2
≥2/1时,2H2S+O2 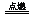 2S+2H2O(H2S过量)
2S+2H2O(H2S过量)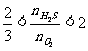 时,两种反应物全部反应完,而产物既有硫又有SO2
时,两种反应物全部反应完,而产物既有硫又有SO2
 逐渐增大
逐渐增大 逐渐减弱
逐渐减弱