18、B 在下列叙述中,能说明盐酸是强酸,醋酸是弱酸的是
A.将pH=4的盐酸和醋酸稀释成pH=5的溶液,醋酸所需加入的pH变大
B.盐酸和醋酸都可用相应的钠盐与浓度硫酸反应制取
C.相同pH的盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸的pH变大
D.相同pH的盐酸和醋酸分别跟锌反应时,产生氢气的起始速率相等
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
|
|
|
|
|
|
|
|
|
|
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
|
|
|
|
|
|
|
|
|
|
第Ⅱ(非选择题 共54分)
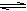 H+ + HA-,HA-
H+ + HA-,HA-
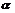 (H2A)>
(H2A)>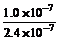 mol/L D.c(OH-)无法确定
mol/L D.c(OH-)无法确定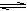 Fe(OH)3
+ 3HCl,若要使FeCl3的水解程度 增大,应采用的方法是
Fe(OH)3
+ 3HCl,若要使FeCl3的水解程度 增大,应采用的方法是