网址:http://m.1010jiajiao.com/timu_id_3837258[举报]
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式K=
| c(CO)c(H2O) |
| c(CO2)c(H2) |
| c(CO)c(H2O) |
| c(CO2)c(H2) |
(2)下列说法中能说明该反应达到平衡状态的是
A.容器中压强不变
B.混合气体中c(CO)不变
C.混合气体的密度不变
D.c(CO)=c(CO2)
E.v(H2)=v(H2O)
F.单位时间内生成CO 的分子数与生成CO2 的分子数相等
(3)830℃时在恒容密闭容器中,以表中所示物质的物质的量(单位为mol)发生上述反应:
| 实验编号 | a(H2) | n(CO2) | n(CO) | n(H2O) |
| A | 2 | 3 | 1 | 5 |
| B | 1 | 1 | 2 | 2 |
| C | 1.2 | 1.2 | 0.8 | 1.8 |
(逆)的是
(14分)在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+ O2 (g)  2SO3(g) △H< 0。查阅资料知SO3熔点16.83℃,沸点44.8℃。
2SO3(g) △H< 0。查阅资料知SO3熔点16.83℃,沸点44.8℃。
(1)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2,O2,SO3物质的量变化如图。
①该反应的化学平衡常数表达式 K=
②该反应能自发进行的原因是 。
③据图判断,该反应处于平衡状态的时间是 。
④据图判断,反应进行至20 min时,曲线发生变化的原因是 (用文字表达)。
(2)某化学研究学习小组用下图的装置组装设计了一个实验,以测定SO2转化为SO3的转化率,仪器的连接顺序是a→h→i→b→c→f→g→d→e。
①为提高SO2的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是 。
②在Ⅰ处用大火加热烧瓶时SO2的转化率会 。(填“填大”“不变”或“减小”)
③用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重 m g,则本实验中SO2的转化率为 。
(14分)在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+
O2 (g)  2SO3(g) △H< 0。查阅资料知SO3熔点16.83℃,沸点44.8℃。
2SO3(g) △H< 0。查阅资料知SO3熔点16.83℃,沸点44.8℃。
(1)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2,O2,SO3物质的量变化如图。

①该反应的化学平衡常数表达式 K=
②该反应能自发进行的原因是 。
③据图判断,该反应处于平衡状态的时间是 。
④据图判断,反应进行至20 min时,曲线发生变化的原因是 (用文字表达)。
(2)某化学研究学习小组用下图的装置组装设计了一个实验,以测定SO2转化为SO3的转化率,仪器的连接顺序是a→h→i→b→c→f→g→d→e。

①为提高SO2的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是 。
②在Ⅰ处用大火加热烧瓶时SO2的转化率会 。(填“填大”“不变”或“减小”)
③用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重 m g,则本实验中SO2的转化率为 。
查看习题详情和答案>>
其化学平衡常数K与温度t的关系如下表,完成下列问题.
| t/℃ | 25 | 125 | 225 | … |
| K | 4.1×105 | K1 | K2 | … |
(2)判断该反应达到化学平衡状态的依据是______(填序号):
A.2VH2(正)=3VNH3(逆)
B.N2的消耗速率等于H2的消耗速率
C. 溶器内压强保持不变
D.混合气体的密度保持不变
E.容器中气体的平均相对分子质量不随时间而变化
F.混合气体的颜色保持不变
(3)将不同量的N2和H2分别通入到体积为2L的恒容密闭容器中,进行上述反应得到如下两组数据:
| 实验组 | 温度(℃) | 起始量(mol) | 平衡量(mol) | 达到平衡所需时间(min) | |
| N2 | H2 | NH3 | |||
| 1 | 650 | 2 | 4 | 0.9 | 9 |
| 2 | 900 | 1 | 2 | 0.3 | 0.01 |
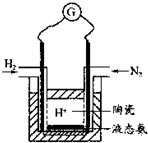
(4)有人设计采用高性能质子导电材料SCY陶瓷(能传递H+),实现了常压下既能合成氨又能发电的实验装置(如图).则其正极的电极反应为______.
在一定体积的密闭容器中,进行如下化学反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g),其化学平衡常数K和温度t的关系如下表:
CO2(g)+H2(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_____________________________,该反应为_______________反应(选吸热或放热)。
若改变条件使平衡向正反应方向移动,则平衡常数_________(填序号)
①一定不变 ②一定减小 ③可能增大 ④增大、减小、不变皆有可能
(2)能判断该反应是否达到化学平衡状态的依据是___________
(a)容器中压强不变 (b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O) (d)c(CO)=c(CO2)
(3)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g) ![]() CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度 /℃ | 起始量/mol | 平衡量/mo | 达到平衡 所需时间 /min | ||
H2O | CO | H2 | CO | |||
1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
3 | 900 | a | b | c | d | t |
实验1中以v(CO2) 表示的反应速率为 。实验2达到平衡所需时间比实验1所需时间短的原因是_________________________________________________________。
查看习题详情和答案>>