摘要:酸性 (1)和NaOH反应 (2)和Na反应
网址:http://m.1010jiajiao.com/timu_id_3836684[举报]
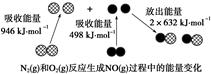
 化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是( )
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是( )
查看习题详情和答案>>
化学反应原理在工业生产中具有十分重要的意义.
(1)工业生产可以用NH3(g)与CO2(g)经过两步反应生成尿素,两步反应的能量变化示意图如图:
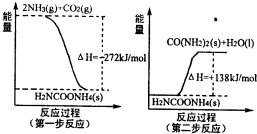
则NH3(g)与CO2(g)反应生成尿素的热化学方程式为 .
(2)已知反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H=akJ.mol-1.测得在不同温度下,该反应的平衡常数K随温度的变化如下:
①该反应的化学平衡常数表达式K= ,a 0(填“>”、“<”或“=”).在500℃2L密闭容器中进行反应,Fe和CO2的起始量均为4mol,则5min后达到平衡时CO2的转化率为
,生成CO的平均速率v(CO)为 .
②700℃反应达到平衡后,要使该平衡向右移动,其他条件不变时,可以采取的措施有 (填字母).
A.缩小反应器容积 B.增加Fe的物质的量
C.升高温度到900℃D.使用合适的催化剂
(3)硫酸厂常用NaOH溶液吸收SO2废气.当吸收液呈中性时,溶液中离子浓度关系正确的是[已知n(SO
):n(HSO
)=1:1时,pH=7.2](填字母) .
A、c(Na+)=2c(SO
)+c(HSO
)
B、c(Na+)>c(HSO
)>c(SO
)>c(H+)=c(OH-)
C、c(Na+)+c(H+)=c(SO
)+c(HSO
)+c(OH-)
查看习题详情和答案>>
(1)工业生产可以用NH3(g)与CO2(g)经过两步反应生成尿素,两步反应的能量变化示意图如图:

则NH3(g)与CO2(g)反应生成尿素的热化学方程式为
(2)已知反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H=akJ.mol-1.测得在不同温度下,该反应的平衡常数K随温度的变化如下:
| 温度/ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
②700℃反应达到平衡后,要使该平衡向右移动,其他条件不变时,可以采取的措施有
A.缩小反应器容积 B.增加Fe的物质的量
C.升高温度到900℃D.使用合适的催化剂
(3)硫酸厂常用NaOH溶液吸收SO2废气.当吸收液呈中性时,溶液中离子浓度关系正确的是[已知n(SO
2- 3 |
- 3 |
A、c(Na+)=2c(SO
2- 3 |
- 3 |
B、c(Na+)>c(HSO
- 3 |
2- 3 |
C、c(Na+)+c(H+)=c(SO
2- 3 |
- 3 |
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是
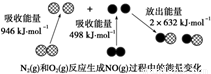
A.1molN2(g)和NA个O2(g)反应放出的能量为180kJ
B.1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量
C.通常情况下,N2(g)和O2(g)混合能直接生成NO
D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
查看习题详情和答案>>
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是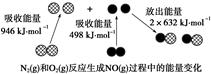
| A.1molN2(g)和NA个O2(g)反应放出的能量为180kJ |
| B.1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量 |
| C.通常情况下,N2(g)和O2(g)混合能直接生成NO |
| D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |