摘要:30.某有机物A可以通过不同的反应制得下列四种有机物: (1)A的结构简式为: .由A制取C的有机反应类型: , (2)由A制B的化学方程式为: . (3)B.C.D.E中 互为同分异构体. (4)A可以与 反应生成D(写任意一种物质的化学式), (5)有关B.C.D.E的叙述中正确的是 . A.四种有机物均为芳香烃 B.有机物E在加热时能与新制的氢氧化铜反应 C.1molB水解时最多可以消耗2molNaOH D.1molC或E最多能与4molH2发生加成反应 31.某同学为测定黄铜矿的纯度(主要成分CuFeS2含少量SiO2).设计如下实验:称取2.0g研细的该黄铜矿样品.高温下和空气中的氧气充分反应: △ 6CuFeS2+19O2 6CuO+2Fe3O4+12SO2 生成的SO2进入D中和水发生反应:SO2+H2O=H2SO3, (1)称量该样品时用的仪器的名称为 . (2)装置A的作用 , a.有利于空气中氧气充分反应 b.除去空气中的水份 c.有利于气体混合 d.有利于观察空气流速 (3)装置B中反应结束后.仍需继续通一段时间空气的目的 . (4)实验后将D中的溶液全部转移至锥形瓶.用1.0mol/L的I2溶液进行滴定.反应为:H2SO3+I2+H2O=H2SO4+2HI.达到终点时消耗I2溶液20.00mL.判断滴定达到终点的现象为 .通过计算.该黄铜矿的纯度为 32.回收的废旧锌锰干电池经过处理后可得到锰粉(主要含MnO2.Mn(OH)2.Fe.NH4Cl和炭黑等).由锰粉制取MnO2的步骤和数据如下: 物质 开始沉淀 沉淀完全 Fe(OH)3 2.7 3.7 Fe(OH)2 7.6 9.6 Fe(OH)2 8.3 9.8 (1)在加热条件下.用浓盐酸浸取锰粉得到含有Mn2+.Fe3+等离子的溶液.MnO2与浓盐酸反应的离子方程式 .该处理方法的缺点 . (2)步骤I中滤渣的化学式 .步骤I中滤渣的化学式 . (3)向步骤I的滤液中加足量H2O2的作用为 .再加NaOH溶液调节pH在3.7<pH<8.3.目的是 . (4)向步骤II的滤液中H2O2溶液.再加NaOH溶液调节pH为9.使Mn2+转化成MnO2.在这一过程中H2O2起 的作用. 33.有一种催化剂为铁的常见的氧化物.为探究该氧化物的成分:
网址:http://m.1010jiajiao.com/timu_id_3831837[举报]
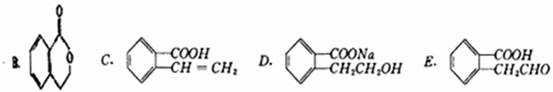
某有机物A可以通过不同的反应制得下列四种有机物:
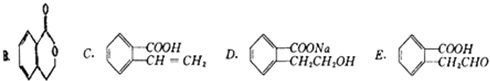
(1)A的结构简式为: ,由A制取C的有机反应类型: ;
(2)由A制B的化学方程式为: .
(3)B、C、D、E中 互为同分异构体.
(4)A可以与 反应生成D(写任意一种物质的化学式);
(5)有关B、C、D、E的叙述中正确的是 .
A.四种有机物均为芳香烃
B.有机物E在加热时能与新制的氢氧化铜反应
C.1molB水解时最多可以消耗2molNaOH
D.1molC或E最多能与4molH2发生加成反应.
查看习题详情和答案>>

(1)A的结构简式为:
(2)由A制B的化学方程式为:
(3)B、C、D、E中
(4)A可以与
(5)有关B、C、D、E的叙述中正确的是
A.四种有机物均为芳香烃
B.有机物E在加热时能与新制的氢氧化铜反应
C.1molB水解时最多可以消耗2molNaOH
D.1molC或E最多能与4molH2发生加成反应.
(16分)某有机物A可以通过不同的反应制得下列四种有机物:
(1)A的结构简式为: ,由A制取C的有机反应类型: ;
(2)由A制B的化学方程式为: 。
(3)B、C、D、E中 互为同分异构体。
(4)A可以与 反应生成D(写任意一种物质的化学式);
(5)有关B、C、D、E的叙述中正确的是 。
A.四种有机物均为芳香烃
B.有机物E在加热时能与新制的氢氧化铜反应
C.1molB水解时最多可以消耗2molNaOH
D.1molC或E最多能与4molH2发生加成反应
查看习题详情和答案>>
(16分)某有机物A可以通过不同的反应制得下列四种有机物: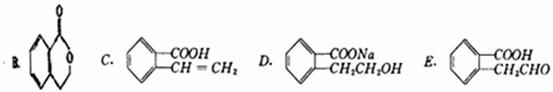
(1)A的结构简式为: ,由A制取C的有机反应类型: ;
(2)由A制B的化学方程式为: 。
(3)B、C、D、E中 互为同分异构体。
(4)A可以与 反应生成D(写任意一种物质的化学式);
(5)有关B、C、D、E的叙述中正确的是 。
A.四种有机物均为芳香烃
B.有机物E在加热时能与新制的氢氧化铜反应
C.1molB水解时最多可以消耗2molNaOH
D.1molC或E最多能与4molH2发生加成反应