摘要:标准状况下下列气体各1g.体积最大的是( ) A 氢气 B 氧气 C 二氧化碳 D 氯气
网址:http://m.1010jiajiao.com/timu_id_3639699[举报]
根据所学知识,完成下列各题:
(1)在标准状况下,气体A的密度为3.17g?L-1,则气体A的摩尔质量为
(2)MgSO4和Al2(SO4)3溶液等体积混合后,Al3+浓度为0.1mol?L-1,SO42-的浓度为0.3mol?L-1.则混合溶液中Mg2+浓度为
(3)7.2g CO和H2的混合气体和适量氧气充入盛有足量过氧化钠的密闭容器中,以连续的电火花引燃,充分反应后,固体质量增重
查看习题详情和答案>>
(1)在标准状况下,气体A的密度为3.17g?L-1,则气体A的摩尔质量为
71g/mol
71g/mol
;(2)MgSO4和Al2(SO4)3溶液等体积混合后,Al3+浓度为0.1mol?L-1,SO42-的浓度为0.3mol?L-1.则混合溶液中Mg2+浓度为
0.15mol/L
0.15mol/L
;(3)7.2g CO和H2的混合气体和适量氧气充入盛有足量过氧化钠的密闭容器中,以连续的电火花引燃,充分反应后,固体质量增重
7.2g
7.2g
g.A和B在一定条件下可合成芳香族化合物E,G在标准状况下是气体,此情况下的密度为1.25g/L.各物质间相互转化关系如下所示:

请回答下列问题:
(1)G中的官能团是
 (用化学式表示),D中的官能团名称是
(用化学式表示),D中的官能团名称是
 .
.
(2)指出反应类型:①
(3)写出化学方程式:A→C
(4)满足下列条件的B的同分异构体有
①遇FeCl3溶液显紫色 ②能发生银镜反应 ③苯环上只有两个取代基.
查看习题详情和答案>>

请回答下列问题:
(1)G中的官能团是


羧基
羧基
,F的结构简式为

(2)指出反应类型:①
酯化反应
酯化反应
,②消去反应
消去反应
,③加聚反应
加聚反应
.(3)写出化学方程式:A→C
2CH3CH2OH+O2
2CH3CHO+H2O
| Cu |
| △ |
2CH3CH2OH+O2
2CH3CHO+H2O
;C与新制的氢氧化铜悬浊液反应:| Cu |
| △ |
CH3CHO+2Cu(OH)2
CH3COOH+Cu2 O↓+2H2O
| △ |
CH3CHO+2Cu(OH)2
CH3COOH+Cu2 O↓+2H2O
.| △ |
(4)满足下列条件的B的同分异构体有
3
3
种.①遇FeCl3溶液显紫色 ②能发生银镜反应 ③苯环上只有两个取代基.
 回答下列各题:
回答下列各题:(1)在探究原电池中电极与电解质溶液之间的关系时,某同学设计了用铝片、铜片作电极,用浓硝酸作电解质溶液的原电池,则铜片为原电池的
负极
负极
极,铝片上的电极反应式为4H++2NO3-+2e-=2NO2↑+2H2O
4H++2NO3-+2e-=2NO2↑+2H2O
.(2)通过
电解池
电解池
装置( 填“原电池”或“电解池”)可以实现如下反应:Cu+2H2O═Cu(OH)2+H2↑
该装置应以铜为
阳极
阳极
极,并可选用下列溶液中的BD
BD
为电解质溶液(填符号).A.H2SO4溶液 B.NaOH溶液 C.CuSO4溶液 D.NaCl溶液
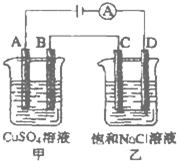
(3)如图所示的两个电解槽中,A、B、C、D均为石墨电极.电解过程中,乙中反应的离子方程式为
2Cl-+2H2O=Cl2↑+H2↑+2OH-
2Cl-+2H2O=Cl2↑+H2↑+2OH-
.若乙烧杯中D极上产生224mL标准状况下的气体,则甲烧杯中B极上可析出铜
0.64
0.64
g(铜的相对原子质量为64).四种短周期元素A、B、C、D的性质或结构信息如下.
信息①原子半径大小:A>B>C>D
信息②四种元素之间形成的某三种分子的比例模型及部分性质:

请根据上述信息回答下列问题.
(1)①C元素在周期表中的位置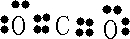
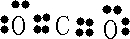 .
.
②A元素的单质与物质甲发生反应的离子方程式
③以Pt为电极,KOH为电解质溶液,两极分别通入乙和C的单质可组成燃料电池,写出电池的电极反应式.负极
(2)A所在周期中,E元素的单质还原性最强,A、E单质反应得到的化合物M是一种重要的化工原料,如图是电解100ml饱和M溶液的装置,X、Y都是惰性电极,实验开始时,同时在两边各滴入几滴酚酞试液,则

①电解池中Y极上的电极反应式
②电解一段时间后,若阴极收集到112ml标准状况下的气体,此时电解液的PH为
查看习题详情和答案>>
信息①原子半径大小:A>B>C>D
信息②四种元素之间形成的某三种分子的比例模型及部分性质:

请根据上述信息回答下列问题.
(1)①C元素在周期表中的位置
第二周期ⅥA族
第二周期ⅥA族
,请写出BC2分子的电子式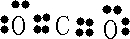
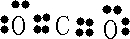
②A元素的单质与物质甲发生反应的离子方程式
Cl2+H2O H++Cl-+HClO
H++Cl-+HClO
 H++Cl-+HClO
H++Cl-+HClOCl2+H2O H++Cl-+HClO
H++Cl-+HClO
. H++Cl-+HClO
H++Cl-+HClO③以Pt为电极,KOH为电解质溶液,两极分别通入乙和C的单质可组成燃料电池,写出电池的电极反应式.负极
CH4-8e-+10OH-=CO32-+7H2O
CH4-8e-+10OH-=CO32-+7H2O
;正极2O2+8e-+4H2O=8OH-
2O2+8e-+4H2O=8OH-
(2)A所在周期中,E元素的单质还原性最强,A、E单质反应得到的化合物M是一种重要的化工原料,如图是电解100ml饱和M溶液的装置,X、Y都是惰性电极,实验开始时,同时在两边各滴入几滴酚酞试液,则

①电解池中Y极上的电极反应式
2Cl-2e-=Cl2↑
2Cl-2e-=Cl2↑
.检验Y电极反应产物的方法是把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色
把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色
.②电解一段时间后,若阴极收集到112ml标准状况下的气体,此时电解液的PH为
13
13
(假设电解液的体积保持不变,常温下)为比较Fe2+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图1中甲、乙所示的实验.请回答下列问题:

(1)定性分析:如图甲可通过观察
(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略.图中仪器A的名称为
(3)某同学要利用乙装置测定某H2O2溶液的物质的量浓度.在锥形瓶中加入0.10mol MnO2粉末后加入50mL 该H2O2溶液,在标准状况下放出气体的体积和时间的关系如图2所示.
①写出H2O2在MnO2作用下发生反应的化学方程式
②实验中放出气体的总体积是
③A、B、C、D各点反应速率快慢的顺序为
④计算H2O2的初始的物质的量浓度
查看习题详情和答案>>

(1)定性分析:如图甲可通过观察
产生气泡的快慢
产生气泡的快慢
定性比较得出结论,有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是消除阴离子不同对实验的干扰
消除阴离子不同对实验的干扰
.(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略.图中仪器A的名称为
分液漏斗
分液漏斗
,实验中需要测量的是产生40mL气体所需的时间
产生40mL气体所需的时间
.(3)某同学要利用乙装置测定某H2O2溶液的物质的量浓度.在锥形瓶中加入0.10mol MnO2粉末后加入50mL 该H2O2溶液,在标准状况下放出气体的体积和时间的关系如图2所示.
①写出H2O2在MnO2作用下发生反应的化学方程式
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
;
| ||
②实验中放出气体的总体积是
60
60
mL;③A、B、C、D各点反应速率快慢的顺序为
D
D
>C
C
>B
B
>A
A
;④计算H2O2的初始的物质的量浓度
0.11mol/L
0.11mol/L
.(结果保留2位小数)