网址:http://m.1010jiajiao.com/timu3_id_276551[举报]
A、B、C、D、E、F六种短周期元素,原子序数依次增大,A、E同主族,D、F同主族,A元素的原子半径是所有原子中最小的,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E、F五种元素都能与D元素形成原子个数比不相同的常见化合物。回答下列问题:
(1)F元素在周期表中的位置 ,
(2)写出阴离子B22-的电子式(用B对应元素的元素符号来表示) 。
(3)常温下,X、Y的水溶液pH均为4,设X、Y水溶液中由水电离出的OH-浓度分别为
a、b,则a与b之比为 。
(4)A、B、D、E四种元素组成的某无机化合物,受热易分解。写出少量该化合物溶液与
足量的Ba(OH)2溶液反应的离子方程式 。
(5)将铝片和镁片用导线连接,插入由A、D、E三种元素组成的化合物的稀溶液中构成
原电池,则负极的电极反应式为 。
(6)A单质与C单质在一定条件下可化合为乙,室温下,向pH=a的乙的水溶液中加入等
体积pH=b的X的水溶液,且a+b=14,充分作用后,该溶液中各种离子浓度由大到小的顺序为 。
查看习题详情和答案>>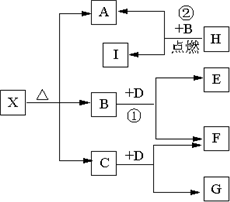 Ⅰ有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A元素的原子是半径最小的原子.B元素的最高价氧化物的水化物与其氢化物反应生成一种盐X,D与A同族,且与E同周期,E元素的最外层电子数是次外层电子数的
Ⅰ有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A元素的原子是半径最小的原子.B元素的最高价氧化物的水化物与其氢化物反应生成一种盐X,D与A同族,且与E同周期,E元素的最外层电子数是次外层电子数的| 3 | 4 |
(1)写出相应元素符合,A
(2)由A、C、D、E四种元素所组成的一种中学常见的化合物,它既能与盐酸反应,又能与NaOH溶液反应,在这种化合物的水溶液中,滴入紫色石蕊试液出现红色,则溶液中离子浓度由大到小的排列顺序为:
(3)将铝片和镁片.插入由A、C、D三种元素组成物质的稀溶液中构成原电池,则负极的电极反应式为
Ⅱ(5分)已知X是一种盐,H是常见金属单质,F、I是常见非金属单质,E、G都是工业上重要的碱性物质,它们有右图所示的关系.
试回答下列问题
(1)G的化学式为:
(2)写出下列反应的化学方程式
①
 2MgO+C
2MgO+C 2MgO+C
2MgO+C纳米氧化镁具有特殊的热、光、电、力学和化学等性能,有广泛的应用前景.如图是利用海水制备纳米氧化镁的流程图.
回答下列问题:
(1)操作I后得到的母液中镁离子浓度为1.8×10-3 mol?L-1,要使镁离子产生沉淀,溶液的pH最低应为______.(已知:Ksp[MgCO3]=6.8×10-6,Ksp[Mg(OH)2]=1.8×10-11)
(2)利用MgCl2?6H2O制备无水氯化镁,需在干燥的______气流中加热,原因是______.
(3)反应I中CO(NH2)2与H2O反应生成CO2和NH3?H2O,还发生另一主要化学反应的离子方程式为______.
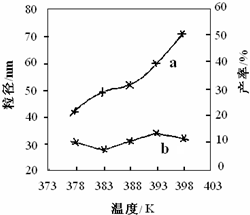
(4)某科研小组研究反应I在温度为378K~398K时的反应时间、反应物配比等因素对制备纳米氧化镁产率的影响.请完成以下实验设计表(表中不要留空格):
| 实验 编号 | T/K | 反应 时间/h | 反应物的物质的量配比 n[CO(NH2)2]:n[MgCl2?6H2O] | 实验目的 |
| ① | 378 | 3 | 3:1 | (Ⅰ)实验①和③探究______ ______; (Ⅱ)实验②和④探究______; (Ⅲ)实验②和______探究反应时间对产率的影响. |
| ② | 378 | 4 | 4:1 | |
| ③ | 378 | 3 | ||
| ④ | 398 | 4 | 4:1 |
 查看习题详情和答案>>
查看习题详情和答案>>
(Ⅰ)现有下列五种物质
A.食盐 B.食醋 C.苹果汁 D.葡萄糖 E.青霉素,请按下列要求填空(填序号)。
富含维生素C的是________;可直接进入血液,补充能量的是_________;应用最广泛的抗生素之一的是________;既可作为调味剂,又可作为防腐剂的是_________;食用过多会引起血压升高、肾脏受损的是_________。
(Ⅱ)抗酸药物的种类很多,其有效成分一般都是碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝和氢氧化镁等化学物质。
(1)抗酸药物具有抗酸作用的原因是__________________________。
(2)某品牌抗酸药的主要成分有糖衣、碳酸镁、氢氧化铝、淀粉。
①写出该抗酸药发挥功效时的离子方程式:
__________________________、__________________________。
②淀粉在抗酸药中作填充剂、黏合剂,淀粉在人体内酶的催化作用下发生水解反应,最终转化为(写分子式)____________________________。
查看习题详情和答案>>