网址:http://m.1010jiajiao.com/timu3_id_274147[举报]
CO(g)十H2O(g)?CO2(g)十H2 (g)△H<0.在850℃时,CO和H2O浓度变化如图;若在t1℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如表.下列说法正确的是:( )

| A、850℃时,按左图所示0~4min用CO2表示的平均反应速率v(CO2)=0.02mol?L-1?min-1 | B、t1℃高于850℃ | C、t1℃时,反应在4min~5min间,平衡向逆反应方向移动,若其它条件不变,可能的原因是增大压强 | D、若t2℃时,各物质的平衡浓度符合c(CO2)?c(H2)=2[c(CO)?c(H2O)],则t2℃高于850℃ |
一定温度下,在一固定体积的容器中,通人一定量的CO和H2O,发生如下反应:CO(g)十H2O(g)![]() CO2(g)十H2 (g);△H<0
CO2(g)十H2 (g);△H<0
(1)在850℃时,CO和H2O浓度变化如下左图,则 0~4min的平均反应速率v(CO)=_ _mol·L-1·min-1

(2)t1℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如右上表。
①计算t1℃该反应的平衡常数为 ,t1℃ 850℃(填大于、小于或等于)。判断依据是________ _______。
②t1℃时,反应在4min—5min间,平衡 移动(填“向左”、“向右”或“不移动”),可能的原因是________。
a.增加CO的浓度 b.增加H2的浓度
c.加压 d.使用催化剂
(3)t2℃时,反应CO2(g)十H2 (g)![]() CO(g)十H2O(g)的平衡浓度符合[CO2]·[H2]=2[CO]·[H2O],则t2℃ 850℃(填大于、小于或等于)。
CO(g)十H2O(g)的平衡浓度符合[CO2]·[H2]=2[CO]·[H2O],则t2℃ 850℃(填大于、小于或等于)。
(12分)一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,
发生如下反应:CO (g) 十H2O (g)  CO2 (g) 十 H2 (g) ; △H<0
CO2 (g) 十 H2 (g) ; △H<0
(1)在850℃时,CO和H2O浓度变化如下左图,则 0~4min的平均反应速率v(CO2)= _mol·L-1·min-1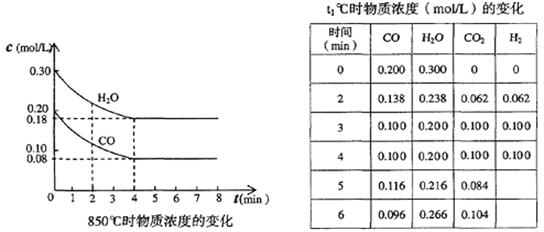
(2)t1℃时,在相同容器中发生上述反应,各物质的浓度变化如右上表:
① 计算t1℃该反应的平衡常数为K = 。
② t1℃时,反应在5min~6min间,平衡 移动(填向左、向右或不 ),若在第5分钟改变一种条件达到第6分钟的浓度,改变的条件是 ________。
(3)t2℃时,化学反应CO (g) + H2O (g)  CO2 (g) + H2 (g)的平衡浓度符合c(CO2)·c(H2)=2 c(CO)·c(H2O),则t2℃ 850℃,判断依据是:
CO2 (g) + H2 (g)的平衡浓度符合c(CO2)·c(H2)=2 c(CO)·c(H2O),则t2℃ 850℃,判断依据是:
一定温度下,在一固定体积的容器中,通人一定量的CO和H2O,发生如下反应:CO(g)十H2O(g)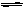 CO2(g)十H2 (g) △H<0。在850℃时,CO和H2O浓度变化如下左图;若在t1℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如右表。下列说法正确的是:
CO2(g)十H2 (g) △H<0。在850℃时,CO和H2O浓度变化如下左图;若在t1℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如右表。下列说法正确的是:
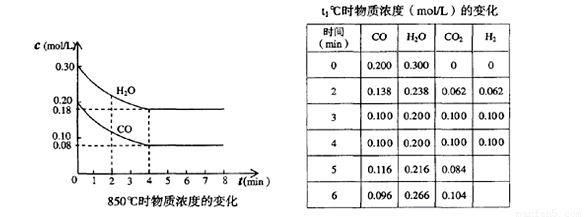
A.850℃时,按左图所示0~4min用CO2表示的平均反应速率v(CO2)=0.02mol·L-1·min-1
B.t1℃高于850℃
C.t1℃时,反应在4min~5min间,平衡向逆反应方向移动,若其它条件不变,可能的原因是增大压强
D.若t2℃时,各物质的平衡浓度符合c(CO2)·c(H2)=2 [c(CO)·c(H2O)],则t2℃高于850℃
查看习题详情和答案>>
(12分)一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,
发生如下反应:CO (g) 十H2O (g)  CO2 (g) 十 H2
(g) ; △H<0
CO2 (g) 十 H2
(g) ; △H<0
(1)在850℃时,CO和H2O浓度变化如下左图,则 0~4min的平均反应速率v(CO2)= _ mol·L-1·min-1
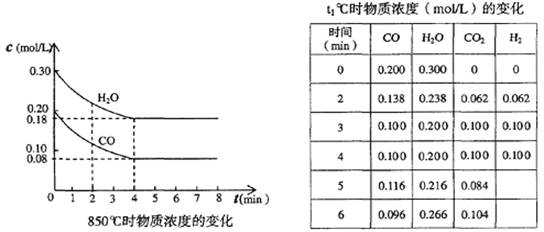
(2)t1℃时,在相同容器中发生上述反应,各物质的浓度变化如右上表:
① 计算t1℃该反应的平衡常数为K = 。
② t1℃时,反应在5min~6min间,平衡 移动(填向左、向右或不 ),若在第5分钟改变一种条件达到第6分钟的浓度,改变的条件是 ________。
(3)t2℃时,化学反应CO (g) + H2O (g)  CO2
(g) + H2 (g)的平衡浓度符合c(CO2)·c(H2)=2 c(CO)·c(H2O),则t2℃ 850℃, 判断依据是:
CO2
(g) + H2 (g)的平衡浓度符合c(CO2)·c(H2)=2 c(CO)·c(H2O),则t2℃ 850℃, 判断依据是:
查看习题详情和答案>>