网址:http://m.1010jiajiao.com/timu3_id_273732[举报]
(1)该反应是__________反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率________(填“增大”“减小”“不变”),原因是______________________________________________。
(3)反应体系中加入催化剂对反应热是否有影响?__________,原因是______________________;
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_________,E2________(填“增大”“减小”“不变”)。
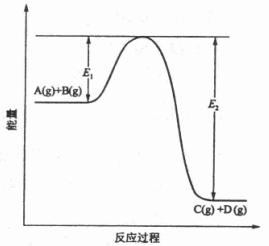
查看习题详情和答案>>反应A(g)+B(g)![]() C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。

(1)该反应是____________________反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率______(填“增大”“减小”“不变”),
原因是____________________________________________;
(3)反应体系中加入催化剂对反应热是否有影响?_______________,原因是_________。
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_________,E2________(填“增大”“减小、”“不变”)。
查看习题详情和答案>>反应A(g)+B(g)C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
(1)该反应是__________反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率________(填“增大”“减小”“不变”),原因是______________________________________________。
(3)反应体系中加入催化剂对反应热是否有影响?______________________,原因是_______________________________________________________;
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_______,E2_______(填“增大”“减小”“不变”)。
查看习题详情和答案>>
22.反应A(g)+B(g) C(g) +D(g)过程中的能量变化如图所示,回答下列问题:
(1)该反应的反应物总能量________生成物的总能量(选填“小于”“大于”或“相等”)。
(2)当反应达到平衡时,若升高温度,A的转化率_____ (选填“增大”“减小”“不变”原因是____________
_ ___________;若增大压强,则V正 V逆(选填“<”“>”“=”)。
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1____ ,E2_____ (填“增大”“减小”“不变”)。
查看习题详情和答案>>
反应A(g)+B(g)C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
(1)该反应是_____________(填“吸热”“放热”)反应。
(2)当反应达到平衡时,升高温度,A的转化率_____________ (填“增大”“减小”或“不变”),
原因是_________________________________________________________________。
(3)反应体系中加入催化剂对反应热是否有影响并说明原因_________________________
___________________________________________。
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:?E1_____________,E2_____________(填“增大”“减小”或“不变”)。
查看习题详情和答案>>