摘要:2.影响饱和汽压大小因素 (1)在相同温度下.不同种类液体饱和汽压一般不同. (2)同一种液体的饱和汽压随液体温度升高而 . (3)同一种液体.在一定温度下.其饱和汽压与饱和汽所占的体积 关. (4)饱和汽压与饱和汽中是否含有其他气体以及含量的多少都没有关系.
网址:http://m.1010jiajiao.com/timu3_id_272769[举报]
(1)在一定温度和压强条件下,影响气体物质体积大小的主要因素有以下两点,即①_________和②_________。
(2)2 mol O3和3 mol O2的质量比为_________,在同温同压条件下的体积比为_________,所含氧原子数目之比为_________。
(3)标准状况下,2 mol CO2的体积是_________ L,该条件下的CO2的密度为_________。
(4)同温同压条件下,相同体积的CH4和O2组成的混合气体中,CH4和O2的质量比为_________,该混合气体的平均摩尔质量为_________,其密度是相同条件下氢气密度的_________倍。
查看习题详情和答案>>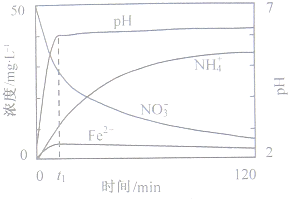 (2011?安徽)地下水中硝酸盐造成的氮污染已成为一个世界性的环节问题.文献报道某课题组模拟地下水脱氮过程,利用Fe粉和KNO3溶液反应,探究脱氮原理及相关因素对脱氮速率的影响.
(2011?安徽)地下水中硝酸盐造成的氮污染已成为一个世界性的环节问题.文献报道某课题组模拟地下水脱氮过程,利用Fe粉和KNO3溶液反应,探究脱氮原理及相关因素对脱氮速率的影响.(1)实验前:①先用0.1mol?L-1H2SO4洗涤Fe粉,其目的是
去除铁粉表面的氧化物等杂质
去除铁粉表面的氧化物等杂质
,然后用蒸馏水洗涤至中性;②将KNO3溶液的pH调至2.5;③为防止空气中的O2对脱氮的影响,应向KNO3溶液中通入N2
N2
(写化学式).(2)图表示足量Fe粉还原上述KNO3溶液过程中,测出的溶液中相关离子浓度、pH随时间的变化关系(部分副反应产物曲线略去).请根据图中信息写出t1时刻前该反应的离子方程式
4Fe+NO3-+10H+═4Fe2++NH4++3H2O
4Fe+NO3-+10H+═4Fe2++NH4++3H2O
.t1时刻后,改反应仍在进行,溶液中NH4+的浓度在增大,Fe2+的浓度却没有增大,可能的原因是生成的Fe2+水解
生成的Fe2+水解
.(3)改课题组对影响脱氮速率的因素提出了如下假设,请你完成假设二和假设三:
假设一:溶液的pH;
假设二:
温度
温度
;假设二:
铁粉颗粒大小
铁粉颗粒大小
;(4)请你设计实验验证上述假设一,写出实验步骤及结论.(已知:溶液中的NO3-浓度可用离子色谱仪测定)
实验结论:
某课外兴趣小组对H2O2的分解速率做了如下实验探究.
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10mL H2O2制取150mLO2所需的时间(秒)

①该研究小组在设计方案时.考虑了浓度、
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响
(2)将质量相同但聚集状态不同的MnO2分别加入到5mL 5%的双氧水中,并用带火星的木条测试.测定结果如下:
①写出H2O2发生的化学反应方程式
②实验结果说明催化剂作用的大小与
查看习题详情和答案>>
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10mL H2O2制取150mLO2所需的时间(秒)

①该研究小组在设计方案时.考虑了浓度、
温度
温度
、催化剂
催化剂
等因素对过氧化氢分解速率的影响.②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响
温度升高化学反应速率加快;反应物浓度增大化学反应速率加快;使用合适的催化剂化学反应速率加快
温度升高化学反应速率加快;反应物浓度增大化学反应速率加快;使用合适的催化剂化学反应速率加快
.(2)将质量相同但聚集状态不同的MnO2分别加入到5mL 5%的双氧水中,并用带火星的木条测试.测定结果如下:
| 催化剂(MnO2) | 操作情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 混合不振荡 | 剧烈反应,带火星的木条复燃 | 3.5分钟 |
| 块状 | 反应较慢,火星红亮但木条未复燃 | 30分钟 |
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
②实验结果说明催化剂作用的大小与
接触面积
接触面积
有关.某课外兴趣小组对H2O2的分解速率做了科学探究采集的数据如下表:
(1)表一:用10mlH2O2制取150mlO2所需时间(秒)
请问:①该研究小组在设计方案时.考虑了浓度、
②从上述影响过氧化氢分解速率的因素中选一个说明该因素对分解速率有何影响?
(2)将质量相同但聚焦状态不同的MnO2分别加入到5ml5%的H2O2中,并用带火星木条测试,测定结果见表二:
③写出H2O2分解的化学方程式
④实验结果说明催化剂作用的大小与
查看习题详情和答案>>
(1)表一:用10mlH2O2制取150mlO2所需时间(秒)
时间(秒) 反应条件 浓度 |
30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
| 无催化剂不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂加热 | 360 | 480 | 540 | 720 |
| MnO2催化剂加热 | 10 | 25 | 60 | 120 |
催化剂
催化剂
、温度
温度
等因素对过氧化氢分解速率的影响.②从上述影响过氧化氢分解速率的因素中选一个说明该因素对分解速率有何影响?
一般加入催化剂,反应速率加快(或,升高温度反应速率加快,降低温度反应速率减慢;增加反应物浓度,反应速率加快,减小反应物浓度,反应速率减慢)
一般加入催化剂,反应速率加快(或,升高温度反应速率加快,降低温度反应速率减慢;增加反应物浓度,反应速率加快,减小反应物浓度,反应速率减慢)
(2)将质量相同但聚焦状态不同的MnO2分别加入到5ml5%的H2O2中,并用带火星木条测试,测定结果见表二:
| 催化剂(MnO2) | 操作情况 | 观察结果 | 反应完成所需及时间 |
| 粉末状 | 混合不振荡 | 剧烈反应、带火星木条复燃 | 3.5分钟 |
| 块状 | 反应较慢,火星红亮但木条未复燃 | 30分钟 |
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
| ||
④实验结果说明催化剂作用的大小与
接触面积
接触面积
有关.