题目内容
2.如图所示,容器A中装有为5×105Pa、温度为300K的理想气体,它由一根吸管和一个关着的阀门与体积是A的四倍的容器B相连;容器B装有压强为1×105Pa、温度为400K的同种理想气体.打开阀门使两边的压强相等,使每个容器的温度保持初始值不变,这时两容器中的气体的压强是多少?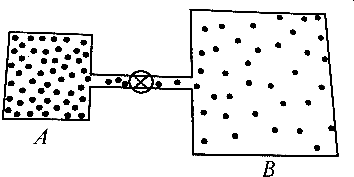
分析 根据理想气体状态方程$\frac{pV}{T}=C$,常数C由物质的量决定,打开阀门前后两容器中气体的总的物质的量不变.
解答 解:设容器A的体积为V,容器B的体积为4V,打开阀门后两边的气体压强为p′,根据理想气体状态方程有:$\frac{pV}{T}=C$
$\frac{{p}_{A}^{\;}V}{{T}_{A}^{\;}}+\frac{{p}_{B}^{\;}×(4V)}{{T}_{B}^{\;}}=\frac{p′V}{{T}_{A}^{\;}}+\frac{p′×(4V)}{{T}_{B}^{\;}}$
代入数据解得:$p′=2×1{0}_{\;}^{5}{p}_{a}^{\;}$
答:两容器中的气体的压强是$2×1{0}_{\;}^{5}{p}_{a}^{\;}$
点评 本题主要考查理想气体状态方程$\frac{pV}{T}=C$,抓住打开阀门前后气体A和B的总的质量不变,对整体运用理想气体状态方程列式即可.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
10.软铁棒放在永磁体的旁边能被磁化,这是由于( )
| A. | 在永磁体磁场作用下,软铁棒中形成了分子电流 | |
| B. | 在永磁体磁场作用下,软铁棒中的分子电流消失了 | |
| C. | 在永磁体磁场作用下,软铁棒中分子电流的取向 变得大致相同 | |
| D. | 在永磁体磁场作用下,软铁棒中分子电流的取向变得更加杂乱无章 |
17. 一质点作直线运动的v-t图象如图所示,下列选项不正确的是( )
一质点作直线运动的v-t图象如图所示,下列选项不正确的是( )
 一质点作直线运动的v-t图象如图所示,下列选项不正确的是( )
一质点作直线运动的v-t图象如图所示,下列选项不正确的是( )| A. | 在0~4s内该质点的平均速度是5m/s | |
| B. | 在1~2s内,质点所受合外力为零 | |
| C. | 在0~1s内该质点的加速度大小大于2~4s内的加速度大小 | |
| D. | 在0~1s内该质点的运动方向与2~4s内的运动方向相反 |
7.为纪念中国航天事业的成就,发扬航天精神,自2016年起,将每年的4月24日设立为“中国航天日”.在46年前的这一天,中国第一颗人造卫星发射成功.若该卫星运行轨道与地面的最近距离为h1,最远距离为h2.已知地球的半径为R,地球表面的重力加速度为g,月球绕地球做匀速圆周运动的周期为T,引力常量为G.根据以上信息可求出的物理量有( )
| A. | 地球的质量 | |
| B. | 月球绕地球做匀速圆周运动的轨道半径 | |
| C. | 中国第一颗人造卫星绕地球运动的周期 | |
| D. | 月球表面的重力加速度 |
14.某高处雨滴无风时落地速度为5m/s,由于受到水平风速的影响,雨滴落地速度与水平地面成30°角,则雨滴落地速度大小为( )
| A. | 5m/s | B. | 5$\sqrt{2}$m/s | C. | 10m/s | D. | 10$\sqrt{3}$m/s |
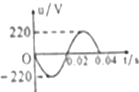 某交流电的电压随时间变化的规律如图所示,此交流电压的有效值为$110\sqrt{2}$V,交流电的频率为25Hz.
某交流电的电压随时间变化的规律如图所示,此交流电压的有效值为$110\sqrt{2}$V,交流电的频率为25Hz. 一质量为1kg的物体由光滑半圆形轨道顶端从静止开始释放,如图4所示,A为轨道最低点,A与圆心0在同一竖直线上,已知圆弧轨道半径为1.8m,求:
一质量为1kg的物体由光滑半圆形轨道顶端从静止开始释放,如图4所示,A为轨道最低点,A与圆心0在同一竖直线上,已知圆弧轨道半径为1.8m,求: 如图所示,一长为L的轻杆,其左端与右端分别固定着质量都是m的A、B两小球,杆可绕离左端$\frac{1}{4}$处的水平轴O无摩擦转动.开始时,将杆拉至水平状态.求杆由静止释放至A球转至最高点的过程中:
如图所示,一长为L的轻杆,其左端与右端分别固定着质量都是m的A、B两小球,杆可绕离左端$\frac{1}{4}$处的水平轴O无摩擦转动.开始时,将杆拉至水平状态.求杆由静止释放至A球转至最高点的过程中: