题目内容
12.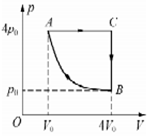 如图所示,一定质量的理想气体,从状态B开始以B→A→C→B的顺序变化.已知气体在状态A时的温度为t(单位为℃),气体从状态B→A的过程中向外放热为Q,试求:
如图所示,一定质量的理想气体,从状态B开始以B→A→C→B的顺序变化.已知气体在状态A时的温度为t(单位为℃),气体从状态B→A的过程中向外放热为Q,试求:①气体在C状态时的温度tC;
②气体实现从状态B→A→C→B的变化过程中,对外做的功.
分析 ①从状态A到状态C为等压变化过程,由盖-吕萨克定律即可求出气体在C状态时的温度tC;
②分析可知TA=TB,故A状态和B状态的内能相等,B到A过程内能变化为0,分别对B到A的过程和A到C的过程利用热力学第一定律,结合等压过程做功公式W=P△V,以及等容过程做功W=0即可求出,每一个过程的做功情况,加和即可求出对外做的总功.
解答 解:①气体从状态A到状态C为等压变化过程;
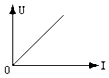
根据图象可知:VA=V0,TA=273+t,VC=4V0,
根据盖-吕萨克定律可得:$\frac{{V}_{A}}{{T}_{A}}$=$\frac{{V}_{C}}{{T}_{C}}$
解得:TC=4TA=4(273+t)=1092+t
化为摄氏温标可得气体在C状态时的温度:tC=819+t
②从B状态到A状态,根据理想气体的状态方程可得:$\frac{{P}_{A}{V}_{A}}{{T}_{A}}$=$\frac{{P}_{B}{V}_{B}}{{T}_{B}}$
可得:TA=TB,故A状态和B状态的内能相等,B到A过程内能变化:△U=0
从B到A的过程根据热力学第一定律可得:△U=W1-Q
所以:W1=Q
A到C过程,等压变化,体积变大,气体对外做功:W2=-4p0(4V0-V0)=-12p0V0,
则,从状态B→A→C→B的变化过程中,对外做的功:W=(-W1)+(-W2)=12p0V0-Q
答:①气体在C状态时的温度tC为819+t;
②气体实现从状态B→A→C→B的变化过程中,对外做的功为12p0V0-Q.
点评 本题考查了气体实验定律和热力学第一定律的综合应用,关键是要能根据图象知道发生何种状态变化过程,选择合适的实验定律,注意理想气体的内能与热力学温度成正比以及每个过程中做功的正负.

练习册系列答案
相关题目
3.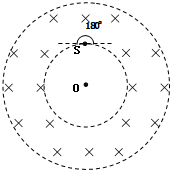 如图,环形区域内有垂直纸面向里的匀强磁场,磁感应强度大小为B,磁场边界为半径为a和2a 的两个同心圆.在小圆上的S处有一粒子源,向磁场在纸面内1800范围内发射相同的带电粒子,粒子带电量为-q,质量为m,速率均为V0,不计粒子重力.设粒子从进入磁场到飞出磁场的时间为t,则( )
如图,环形区域内有垂直纸面向里的匀强磁场,磁感应强度大小为B,磁场边界为半径为a和2a 的两个同心圆.在小圆上的S处有一粒子源,向磁场在纸面内1800范围内发射相同的带电粒子,粒子带电量为-q,质量为m,速率均为V0,不计粒子重力.设粒子从进入磁场到飞出磁场的时间为t,则( )
 如图,环形区域内有垂直纸面向里的匀强磁场,磁感应强度大小为B,磁场边界为半径为a和2a 的两个同心圆.在小圆上的S处有一粒子源,向磁场在纸面内1800范围内发射相同的带电粒子,粒子带电量为-q,质量为m,速率均为V0,不计粒子重力.设粒子从进入磁场到飞出磁场的时间为t,则( )
如图,环形区域内有垂直纸面向里的匀强磁场,磁感应强度大小为B,磁场边界为半径为a和2a 的两个同心圆.在小圆上的S处有一粒子源,向磁场在纸面内1800范围内发射相同的带电粒子,粒子带电量为-q,质量为m,速率均为V0,不计粒子重力.设粒子从进入磁场到飞出磁场的时间为t,则( )| A. | 若V0=$\frac{qBa}{m}$,t最小为$\frac{πm}{3qB}$ | B. | 若V0=$\frac{qBa}{m}$,t最大为$\frac{4mπ}{3qB}$ | ||
| C. | 若V0=$\frac{2qBa}{m}$,t一定大于$\frac{πm}{6qB}$ | D. | 若V0=$\frac{2qBa}{m}$,t一定小于$\frac{πm}{2qB}$ |
17. 如图所示,一蹦极运动员身系弹性蹦极绳从水面上方的高台下落,到最低点时距水面还有数米距离.假定空气阻力可忽略,运动员可视为质点,从蹦极绳刚拉直开始到运动员下落至最低点的过程中,下列判断不正确的是( )
如图所示,一蹦极运动员身系弹性蹦极绳从水面上方的高台下落,到最低点时距水面还有数米距离.假定空气阻力可忽略,运动员可视为质点,从蹦极绳刚拉直开始到运动员下落至最低点的过程中,下列判断不正确的是( )
 如图所示,一蹦极运动员身系弹性蹦极绳从水面上方的高台下落,到最低点时距水面还有数米距离.假定空气阻力可忽略,运动员可视为质点,从蹦极绳刚拉直开始到运动员下落至最低点的过程中,下列判断不正确的是( )
如图所示,一蹦极运动员身系弹性蹦极绳从水面上方的高台下落,到最低点时距水面还有数米距离.假定空气阻力可忽略,运动员可视为质点,从蹦极绳刚拉直开始到运动员下落至最低点的过程中,下列判断不正确的是( )| A. | 运动员的动能先增大后减小 | |
| B. | 运动员重力势能始终减小 | |
| C. | 运动员克服弹力做功,蹦极绳弹性势能增加 | |
| D. | 运动员重力势能的改变量数值上等于弹性势能的改变量 |
4. 如图所示,小球从高处下落到竖直放置的轻弹簧上,那么小球从接触弹簧开始到将弹簧压缩到最短的过程中(弹簧保持竖直),下列关于能的叙述正确的是(不计空气阻力)( )
如图所示,小球从高处下落到竖直放置的轻弹簧上,那么小球从接触弹簧开始到将弹簧压缩到最短的过程中(弹簧保持竖直),下列关于能的叙述正确的是(不计空气阻力)( )
 如图所示,小球从高处下落到竖直放置的轻弹簧上,那么小球从接触弹簧开始到将弹簧压缩到最短的过程中(弹簧保持竖直),下列关于能的叙述正确的是(不计空气阻力)( )
如图所示,小球从高处下落到竖直放置的轻弹簧上,那么小球从接触弹簧开始到将弹簧压缩到最短的过程中(弹簧保持竖直),下列关于能的叙述正确的是(不计空气阻力)( )| A. | 弹簧的弹性势能不断增大 | B. | 小球的动能先增大后减小 | ||
| C. | 小球的重力势能先增大后减小 | D. | 小球的机械能总和保持不变 |
2.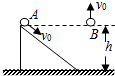 如图所示,小物体A沿高为h、倾角为θ的光滑斜面以初速度v0从顶端滑到底端,而相同的物体B以同样大小的初速度从同等高度处竖直上抛,不计空气阻力.则( )
如图所示,小物体A沿高为h、倾角为θ的光滑斜面以初速度v0从顶端滑到底端,而相同的物体B以同样大小的初速度从同等高度处竖直上抛,不计空气阻力.则( )
 如图所示,小物体A沿高为h、倾角为θ的光滑斜面以初速度v0从顶端滑到底端,而相同的物体B以同样大小的初速度从同等高度处竖直上抛,不计空气阻力.则( )
如图所示,小物体A沿高为h、倾角为θ的光滑斜面以初速度v0从顶端滑到底端,而相同的物体B以同样大小的初速度从同等高度处竖直上抛,不计空气阻力.则( )| A. | 两物体落地时速率相同 | |
| B. | 两物体落地时重力做功的瞬时功率PA=PB | |
| C. | 两物体落地时重力做功的瞬时功率PA<PB | |
| D. | 从开始运动至落地过程中,重力对它们做得功的平均功率一定相同 |
 如图所示,虚线PQ、MN间存在如图所示的水平匀强电场,一带电粒子质量为m=2.0×10-11 kg、电荷量为q=+1.0×10-5C,从a点由静止开始经电压为U=100V的电场加速后,从C点垂直于电场线进入匀强电场E中,从虚线MN上的某点b(图中未画出)离开匀强电场时速度与电场方向成30°角.已知PQ、MN间距离为20cm,带电粒子的重力忽略不计.求:
如图所示,虚线PQ、MN间存在如图所示的水平匀强电场,一带电粒子质量为m=2.0×10-11 kg、电荷量为q=+1.0×10-5C,从a点由静止开始经电压为U=100V的电场加速后,从C点垂直于电场线进入匀强电场E中,从虚线MN上的某点b(图中未画出)离开匀强电场时速度与电场方向成30°角.已知PQ、MN间距离为20cm,带电粒子的重力忽略不计.求: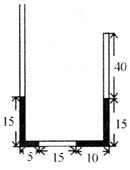 竖直放置粗细均匀的U形细玻璃管两臂分别灌有水银,水平管部分有一空气柱,各部分长度如图所示,单位为厘米.现将管的右端封闭,从左管口缓慢倒入水银,恰好使右侧的水银全部进入右管中,已知大气压强p0=75cmHg,环境温度不变,左管足够长.求:
竖直放置粗细均匀的U形细玻璃管两臂分别灌有水银,水平管部分有一空气柱,各部分长度如图所示,单位为厘米.现将管的右端封闭,从左管口缓慢倒入水银,恰好使右侧的水银全部进入右管中,已知大气压强p0=75cmHg,环境温度不变,左管足够长.求: