题目内容
2.在容积为40L的容器中,盛有压缩二氧化碳3.96kg,该容器能承受的压强不超过6.0×106pa,求容器会有爆炸危险时内部气体达到的摄氏温度?(已知二氧化碳在标准状态下的密度是1.98kg/m3,温度是0℃,压强是1×105pa)分析 已知二氧化碳的质量和标准状况下的密度,即可求出标准状况下的气体的体积,然后结合容器能承受的最大压强,结合理想气体的状态方程即可求出.
解答 解:容器内的气体在标准状态下的状态量分别为:
T1=273K,p1=1×105pa,V1=ρm=1.98×3.96=2m3
气体达到爆炸点的状态量为:
p2=6.0×106pa,V2=40L=0.04m3
根据理想气体状态方程列式:$\frac{{P}_{1}{V}_{1}}{{T}_{1}}=\frac{{P}_{2}{V}_{2}}{{T}_{2}}$
代入数据解得:
T2=327.6K
即:t2=54.6℃
答:容器会有爆炸危险时内部气体达到的摄氏温度是54.6℃.
点评 该题考查理想气体的状态方程,解得的关键是根据标准状况下气体的密度求出标准状况下气体的体积,然后才能使用气态方程.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
1.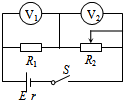 如图所示,电源内阻不能忽略,R1为定值电阻,R2为滑动变阻器,电压表和电流表均为理想电表.当滑动变阻器的触头向右滑动时,V1示数变化量的绝对值为|△U1|,V2示数变化量的绝对值为|△U2|.下列说法正确的是( )
如图所示,电源内阻不能忽略,R1为定值电阻,R2为滑动变阻器,电压表和电流表均为理想电表.当滑动变阻器的触头向右滑动时,V1示数变化量的绝对值为|△U1|,V2示数变化量的绝对值为|△U2|.下列说法正确的是( )
 如图所示,电源内阻不能忽略,R1为定值电阻,R2为滑动变阻器,电压表和电流表均为理想电表.当滑动变阻器的触头向右滑动时,V1示数变化量的绝对值为|△U1|,V2示数变化量的绝对值为|△U2|.下列说法正确的是( )
如图所示,电源内阻不能忽略,R1为定值电阻,R2为滑动变阻器,电压表和电流表均为理想电表.当滑动变阻器的触头向右滑动时,V1示数变化量的绝对值为|△U1|,V2示数变化量的绝对值为|△U2|.下列说法正确的是( )| A. | 电流表A的示数变小,电压表V1的示数变大 | |
| B. | 电压表V1、V2的示数都变小 | |
| C. | |△U1|=|△U2| | |
| D. | |△U1|<|△U2| |
7.在探究“加速度与力、质量的关系”活动中:
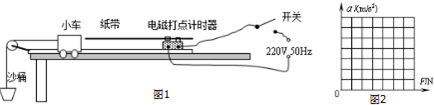
(1)将实验器材组装如图1所示.请你指出该装置中的错误或不妥之处:
①电源电压使用220V;
②没有平衡摩擦力;
③小车没有靠近打点计时器.
(2)纠正实验装置后,该同学顺利完成了实验.在实验中保持小车质量不变,改变沙桶的质量,测得小车所受绳子的拉力F和加速度a的数据如下表:
①根据测得的数据,在图2中作出a-F图象;
②由图象可知,小车与长木板之间的最大静摩擦力大小为0.12N.

(1)将实验器材组装如图1所示.请你指出该装置中的错误或不妥之处:
①电源电压使用220V;
②没有平衡摩擦力;
③小车没有靠近打点计时器.
(2)纠正实验装置后,该同学顺利完成了实验.在实验中保持小车质量不变,改变沙桶的质量,测得小车所受绳子的拉力F和加速度a的数据如下表:
| F/N | 0.21 | 0.30 | 0.40 | 0.49 | 0.60 |
| a/(ms-2) | 0.10 | 0.21 | 0.29 | 0.41 | 0.49 |
②由图象可知,小车与长木板之间的最大静摩擦力大小为0.12N.
14.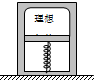 如图所示,在水平面上放置着一个密闭绝热的容器,容器内一个有质量的活塞封闭着理想气体,活塞下部为真空.两端固定的轻弹簧被压缩后用绳扎紧.现在绳突然断开,当轻弹簧推动活塞上升的过程中,理想气体( )
如图所示,在水平面上放置着一个密闭绝热的容器,容器内一个有质量的活塞封闭着理想气体,活塞下部为真空.两端固定的轻弹簧被压缩后用绳扎紧.现在绳突然断开,当轻弹簧推动活塞上升的过程中,理想气体( )
 如图所示,在水平面上放置着一个密闭绝热的容器,容器内一个有质量的活塞封闭着理想气体,活塞下部为真空.两端固定的轻弹簧被压缩后用绳扎紧.现在绳突然断开,当轻弹簧推动活塞上升的过程中,理想气体( )
如图所示,在水平面上放置着一个密闭绝热的容器,容器内一个有质量的活塞封闭着理想气体,活塞下部为真空.两端固定的轻弹簧被压缩后用绳扎紧.现在绳突然断开,当轻弹簧推动活塞上升的过程中,理想气体( )| A. | 压强增大,温度升高 | B. | 压强增大,温度降低 | ||
| C. | 压强减小,温度升高 | D. | 压强减小,温度降低 |
11.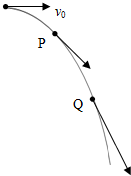 如图所示,小球以v0=5m/s的速度水平抛出,飞行过程中经过空中的P、Q两点,小球在P点时的速度方向与水平方向的夹角为45°,小球在Q点时的速度方向与水平方向的夹角为60°(空气阻力忽略不计,g取10m/s2 ),以下正确的是( )
如图所示,小球以v0=5m/s的速度水平抛出,飞行过程中经过空中的P、Q两点,小球在P点时的速度方向与水平方向的夹角为45°,小球在Q点时的速度方向与水平方向的夹角为60°(空气阻力忽略不计,g取10m/s2 ),以下正确的是( )
 如图所示,小球以v0=5m/s的速度水平抛出,飞行过程中经过空中的P、Q两点,小球在P点时的速度方向与水平方向的夹角为45°,小球在Q点时的速度方向与水平方向的夹角为60°(空气阻力忽略不计,g取10m/s2 ),以下正确的是( )
如图所示,小球以v0=5m/s的速度水平抛出,飞行过程中经过空中的P、Q两点,小球在P点时的速度方向与水平方向的夹角为45°,小球在Q点时的速度方向与水平方向的夹角为60°(空气阻力忽略不计,g取10m/s2 ),以下正确的是( )| A. | P点距离抛出点的距离为2.5m | |
| B. | Q点距离抛出点的水平距离为2.5m | |
| C. | P、Q两点间的高度差h=2.5 m | |
| D. | 小球经过P、Q两点间的时间间隔t=($\sqrt{3}$-1)s |
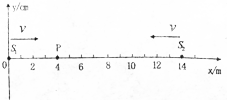 如图所示,均匀介质中取一个坐标轴x,其上有S1、S2两个波源,它们的坐标分别为x1=0,x2=14m,质点P位于x轴上xP=4m处,t=0时刻两波源同时开始由平衡位置向y轴正方向振动,振动周期为T=0.1s,传播速度均匀v=40m/s,波源S1、S2的振幅均为A=2cm,则经过0.1s由波源S1发出的波恰好到达P点.从t=0至t=0.35s内质点P通过的路程为12cm.
如图所示,均匀介质中取一个坐标轴x,其上有S1、S2两个波源,它们的坐标分别为x1=0,x2=14m,质点P位于x轴上xP=4m处,t=0时刻两波源同时开始由平衡位置向y轴正方向振动,振动周期为T=0.1s,传播速度均匀v=40m/s,波源S1、S2的振幅均为A=2cm,则经过0.1s由波源S1发出的波恰好到达P点.从t=0至t=0.35s内质点P通过的路程为12cm.