0 99632 99640 99646 99650 99656 99658 99662 99668 99670 99676 99682 99686 99688 99692 99698 99700 99706 99710 99712 99716 99718 99722 99724 99726 99727 99728 99730 99731 99732 99734 99736 99740 99742 99746 99748 99752 99758 99760 99766 99770 99772 99776 99782 99788 99790 99796 99800 99802 99808 99812 99818 99826 203614
 8Na2CrO4+2Fe2O3+8CO2 ②2Na2CrO4+H2SO4
8Na2CrO4+2Fe2O3+8CO2 ②2Na2CrO4+H2SO4 Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O Ce、
Ce、 Ce、
Ce、 Ce、
Ce、 Ce它们互称为同素异形体
Ce它们互称为同素异形体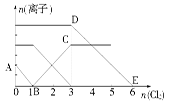
 3NaCl + NaClO4;NaClO4
3NaCl + NaClO4;NaClO4 NaCl + 2O2↑
NaCl + 2O2↑
 MnCl2+Cl2↑+2H2O。其中KMnO4和一般浓度的盐酸即可反应,K2Cr2O7需和较浓盐酸(>6 mol·L-1)反应,MnO2需和浓盐酸(>8 mol·L-1)反应。根据以上信息,下列结论中不正确的是 ( )。
MnCl2+Cl2↑+2H2O。其中KMnO4和一般浓度的盐酸即可反应,K2Cr2O7需和较浓盐酸(>6 mol·L-1)反应,MnO2需和浓盐酸(>8 mol·L-1)反应。根据以上信息,下列结论中不正确的是 ( )。