工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下处理措施和方法正确的是( )。
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 废酸 | 加生石灰中和 | 物理法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含苯废水 | 用活性炭吸附 | 物理法 |
| D | 含纯碱的废水 | 加石灰水反应 | 化学法 |
广东正在建设海洋强省。下列说法不正确的是( )。
| A.从海带中提取碘单质的过程涉及氧化还原反应 |
| B.往淡水中加入NaCl等配成人造海水,可用于海产品的长途运输 |
| C.赤潮主要是由工农业生产和生活废水引起沿海水域的富营养化而造成的 |
| D.海洋经济专属区的资源开发可获得Fe、Co、K、Au、Mg、B等金属 |
下列关于煤、石油、天然气等资源的说法正确的是( )。
| A.石油裂化得到的汽油是纯净物 |
| B.石油产品都可用于聚合反应 |
| C.天然气是一种清洁的化石燃料 |
| D.水煤气是通过煤的液化得到的气体燃料 |
天然海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子。火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如下图所示:
下列说法错误的是( )。
| A.天然海水pH≈8的原因是海水中的CO32-、HCO3-水解 |
| B.“氧化”是利用氧气将H2SO3、HSO3-、SO32-等氧化生成SO42- |
| C.“反应、稀释”时加天然海水的目的是中和、稀释经氧气氧化后海水中生成的酸 |
| D.“排放”出来的海水中SO42-的物质的量浓度与进入吸收塔的天然海水相同 |
下列关于海水知识不正确的是( )。
| A.海水资源的利用包括海水水资源利用和化学资源利用 |
| B.海水既苦又涩,不能直接利用 |
| C.海水中某些金属元素总储量很大,但富集程度却很低 |
| D.海水淡化应同化工生产结合,同能源技术结合 |
下列说法中不正确的是( )。
| A.金属的冶炼原理,就是运用氧化还原反应原理,在一定条件下将金属从其化合物中还原出来 |
| B.冶炼金属时,必须加入一种物质作还原剂 |
| C.金属由化合态变为游离态,一定是被还原 |
| D.金属单质被发现和应用的越早,其活动性越弱 |
热还原法冶炼金属的反应一定是( )。
| A.置换反应 | B.分解反应 | C.复分解反应 | D.氧化还原反应 |
下列金属的工业制法正确的是 ( )。
| A.制钛:用金属钠置换出氯化钛(TiCl4)溶液中的钛 |
| B.炼铁:用焦炭和空气反应产生的一氧化碳在高温下还原铁矿石中的铁 |
| C.制钠:用海水作原料制得精盐,再电解纯净氯化钠溶液得到金属钠 |
| D.炼铜:用黄铜矿经电解精炼得到纯度为99.9%的铜 |
在冶金工业上,均不能用通常化学还原剂制得的金属组是 ( )。
| A.Na,Ba,Mg,Al | B.Na,K,Zn,Fe |
| C.Zn,Fe,Cu,Ag | D.Mg,Al,Zn,Fe |
根据海水综合利用的工业流程图(如图),判断下列说法正确的是( )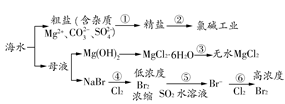
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
| A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 |
| B.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.在过程④、⑥反应中每氧化0.2 mol Br-,需消耗2.24 L Cl2 |
| D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 |