向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是
| | 操作 | 现象 | 结论 |
| A | 滴加BaCl2溶液 | 生成白色沉淀 | 原溶液中有SO42- |
| B | 滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+、无K+ |
| D | 滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
有编号为A、B、C、D的四瓶无色液体,仅知道是1%酚酞、0.1mol·L-1NaOH溶液、0.1mol·L-1盐酸和0.1mol·L-1NaCl溶液。化学老师现要求甲、乙、丙、丁四位学生对它们进行鉴别,规定每人只需鉴别两瓶溶液,如果两瓶溶液鉴别都正确,得满分,如果只有一瓶鉴别正确,则算及格。以下是四位学生的鉴别结果:
| A | A为0.1mol·L -1盐酸 | D为0.lmol·L-1NaCl溶液 | 老师评价:四位学生都及格,但是没有一个得满分 |
| B | A为0.1mol·L -1NaOH溶液 | C为0.1mol·L-1盐酸 | |
| C | A为1%酚酞 | B为0.1mol·L-1盐酸 | |
| D | D为0.1mol·L-1盐酸 | B为0.1mol·L-1 NaOH溶液 |
下列结论正确的是
A.A为1%酚酞 B.B为0.1mol·L-1NaCl溶液
C.C为0.1mol·L-1NaOH溶液 D.D为0.1mol·L-1盐酸
如下图所示,利用海水可提取很多重要的化工原料。
下列有关说法正确的是.( )。
| A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| B.第②步中工业上可采用石墨为阴极,铁为阳极,采用阳离子交换膜的电解装置 |
| C.第③步中结晶出的MgCl2·6H2O可在空气中受热分解制无水MgCl2 |
| D.在第④步中溴元素被氧化,第⑤、⑥步中既有溴元素被氧化也有溴元素被还原 |
下列鉴别方法可行的是
| A.用NH3·H2O溶液鉴别Al3+、Mg2+和Ag+ |
| B.用Ba(NO3)2溶液鉴别Cl—、SO2—4和CO2—3 |
| C.用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷 |
| D.用新制氢氧化铜悬浊液鉴别甲醛和甲酸甲酯 |
为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序
①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;
⑤加过量BaCl2溶液。
| A.④②⑤ | B.②⑤④①③ | C.④①②⑤③ | D.①④②⑤③ |
现有三组溶液:①汽油和氯化钠溶液,②酒精和水的混合溶液,③氯化钠和单质溴的溶液,以上混合溶液分离的正确方法依次是
| A.分液、萃取、蒸馏 | B.萃取、蒸馏、分液 |
| C.分液、蒸馏、萃取 | D.蒸馏、萃取、分液 |
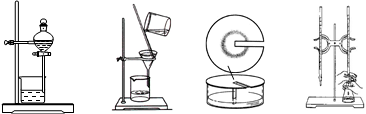
下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是
| A.蒸馏、蒸发、萃取、过滤 | B.蒸馏、过滤、萃取、蒸发 |
| C.萃取、过滤、蒸馏、蒸发 | D.过滤、蒸发、萃取、蒸馏 |
下列实验不能达到实验目的的是
| A.用结晶法提纯混有少量氯化钾的硝酸钾 |
| B.用KSCN检验溶液中Fe3+的存在 |
| C.用湿润的淀粉碘化钾试纸检验氯气 |
| D.用酒精萃取碘水中的碘 |
根据下图海水综合利用的工业流程图,判断下列说法正确的是
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
| A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 |
| B.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.在过程④、⑥反应中每氧化0.2 mol Br- 需消耗2. 24 L Cl2 |
| D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 |