下列说法正确的是
| A.在中和热的测定实验中,将氢氧化钠溶液迅速倒入盛有盐酸的量热计中,立即读出并记录溶液的起始温度,充分反应后再读出并记录反应体系的最高温度 |
| B.用纸层析法分离Cu2+和Fe3+,滤纸上端呈棕黄色,说明Fe3+在有机溶剂中的溶解能力较Cu2+小 |
| C.阿司匹林制备实验中,将粗产品加入饱和NaOH溶液中以除去水杨酸聚合物 |
| D.银氨溶液不能留存,久置后会变成氮化银,容易爆炸 |
在含有Ag+的酸性溶液中,以铁铵矾NH4Fe(SO4)2作指示剂,用KSCN的标准溶液滴定Ag+。已知:AgSCN (白色s)  Ag+ + SCN-,Ksp="1.0" ×10-12 ;Fe3+ + SCN-
Ag+ + SCN-,Ksp="1.0" ×10-12 ;Fe3+ + SCN-  FeSCN2+ (红色), K=138
FeSCN2+ (红色), K=138
下列说法不正确的是
| A.边滴定,边摇动溶液,溶液中首先析出AgSCN白色沉淀 |
| B.当Ag+定量沉淀后,少许过量的SCN-与Fe3+生成红色配合物,即为终点 |
| C.上述实验可用KCl标准溶液代替KSCN的标准溶液滴定Ag+ |
| D.滴定时,必须控制溶液一定的酸性,防止Fe3+水解,影响终点的观察 |
关于下列各实验装置的叙述中,错误的是( )
| A.装置①可用于分离C2H5OH和H2O的混合物 |
| B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 |
| C.装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 |
| D.装置④可用于干燥、收集NH3,并吸收多余的NH3 |
实验室用标准盐酸测定未知浓度NaOH溶液,用甲基橙作指示剂,下列操作可能使测定结果偏低的是( )
| A.酸式滴定管在装酸液前未用标准酸液润洗 |
| B.开始时酸式滴定管尖嘴部分留有气泡,滴定过程中消失 |
| C.锥形瓶内溶液颜色由黄变橙时立即停止滴定 |
| D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次 |
下述实验不能达到预期实验目的的是( )
| 序号 | 实验内容 | 实验目的 |
| A | 将2.5gCuSO4·5H2O溶解在97.5g水中 | 配制质量分数为1.6%的CuSO4溶液 |
| B | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
| C | 室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
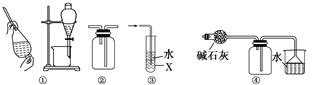
下列实验装置能达到实验目的的是(夹持仪器未画出)
| A.①装置用于检验1-溴丙烷消去产物 | B.②装置用于石油的分馏 |
| C.③装置用于实验室制硝基苯 | D.④装置可证明酸性:盐酸>碳酸>苯酚 |
下列制备气体的实验设计中错误的是( )
| 选项 | A | B | C | D |
| 药品 | NH4Cl 与Ca(OH)2 | 石灰石和 稀盐酸 | 稀硝酸 和铜片 | KMnO4 与浓盐酸 |
| 装置 |  |  |  |  |
以下实验原理或操作中,正确的是( )
| A.除去CO2中混有的少量CO,通入适量O2后点燃 |
| B.焰色反应实验前,先用稀硫酸洗净并灼烧铂丝 |
| C.用pH试纸测定硝酸的pH |
| D.用洗净后未干燥的锥形瓶进行中和滴定实验 |
下列有关实验的操作及描述不正确的是( )
| A.用托盘天平称取10.5 g NaCl时应在右边托盘中放入10 g砝码 |
| B.粗盐提纯时,为了加快过滤速率,可用玻璃棒搅拌过滤器中的液体 |
| C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.测定溶液pH的操作:将pH试纸置于表面皿上,用玻璃棒蘸取溶液,点在pH试纸的中部,然后与标准比色卡对照 |

