NOx是汽车尾气中的主要污染物之一。通过NOx传感器可监测NOx的含量,其工作原理示意图如下。下列说法正确的是
| A.Pt电极作负极,NiO电极作正极 |
| B.Pt电极上发生的是氧化反应 |
| C.NiO电极上发生的是还原反应 |
| D.NiO电极的电极反应式为NO+O2–-2e–=NO2 |
臭氧是常见的强氧化剂,广泛用于水处理系统。制取臭氧的方法很多,其中高压放电法和电解纯水法原理如下图所示,下列有关说法不正确的是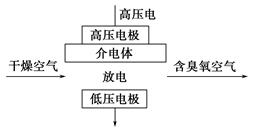
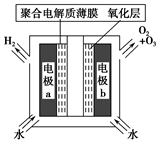
A.高压放电法,反应的原理为3O2 2O3 2O3 |
| B.高压放电出来的空气中,除含臭氧外还含有氮的氧化物 |
| C.电解时,电极b周围发生的电极反应有3H2O-6e-=O3↑+6H+和2H2O-4e-=O2↑+4H+ |
| D.电解时,H+由电极a经聚合固体电解质膜流向电极b |
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是
| A.用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl--2e-=Cl2↑ |
| B.氢氧燃料电池的负极反应式:O2+2H2O+4e-=4OH- |
| C.粗铜精炼时,与电源正极相连的是纯铜,阳极反应式为Cu-2e-=Cu2+ |
| D.钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+ |
下列事实解释准确的是
| A.糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。脱氧过程中铁作原电池正极,电极反应为:Fe-2 e-=Fe2+ |
| B.酸性氢氧燃料电池的正极电极反应为:2H2O+O2+4e-=4OH- |
| C.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,该反应的△S>0,说明反应△H>0 |
| D.铅蓄电池的正极反应为:PbO2+4H++2 e-=Pb2++2H2O |
关于下列装置说法正确的是
| A.装置①中,盐桥中的K+移向CuSO4溶液 |
| B.装置①中,Zn为负极,发生还原反应 |
| C.装置②中的Fe发生析氢腐蚀 |
| D.装置②中电子由Fe流向石墨,然后再经溶液流向Fe |
由化学能转化的热能或电能仍然是人类使用的主要能源。根据下图所示的装置,判断下列说法不正确的是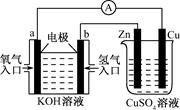
| A.该装置中Cu极为阳极 |
| B.当铜片的质量变化了12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L |
| C.该装置中b极的电极反应式是:H2+2OH--2e- = 2H2O |
| D.该装置中a极为正极,发生氧化反应 |
用惰性电极分别电解下列各物质的水溶液一段时间后,向剩余溶液中加入适量水能使溶液恢复到电解前浓度的是
| A.CuSO4 | B.Na2SO4 | C.CuCl2 | D.NaCl |
关于右图电化学装置中的电极名称、材料及反应均可能正确的是 ( )
| A.阴极(Cu片)2C1――2e-=Cl2↑ |
| B.阳极(Cu片):4OH――4e-=2H2O+O2↑ |
| C.正极(石墨棒):Fe3+ +e-= Fe2+ |
| D.负极(Fe钉):Fe-3e-=Fe3+ |
电浮选凝聚法处理污水的原理如图所示。电解过程生成的胶体能使污水中的悬浮物凝聚成团而除去,电解时阳极也会产生少量气体。下列说法正确的是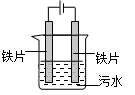
| A.可以用铝片或铜片代替铁片 |
| B.阳极产生的气体可能是O2 |
| C.电解过程中H+向阳极移动 |
| D.若污水导电能力较弱,可加入足量硫酸 |
