钢铁防腐方法有许多种,如图是其中的一种方法,描述正确的是( )
| A.图中所示是牺牲阳极的阴极保护法 |
| B.铁闸门作阴极,发生还原反应 |
| C.电子流向:a→铁闸门→辅助电极→b |
| D.辅助电极上的反应:O2+2H2O+4e-=4OH- |
将KCl和CuSO4两种溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图所示,则下列说法正确的是 ( )。
| A.整个过程中两电极反应2Cl--2e-=Cl2↑、2H++2e-=H2↑不可能同时发生 |
| B.电解至c点时,往电解液中加入适量CuCl2固体,即可使电解液恢复至原来的浓度 |
| C.ab段表示电解过程中H+被还原,pH上升 |
| D.原混合溶液中KCl和CuSO4的浓度之比恰好为2∶1 |
体积为1 L的某溶液中含有的离子如表所示:
| 离子 | Cu2+ | Al3+ | NO3- | Cl- |
 | 1 | 1 | a | 1 |
用Pt电极电解该溶液,当电路中有3 mol电子通过时(忽略电解时溶液体积的变化及电解产物可能存在的溶解现象),下列说法正确的是 ( )。
A.电解后溶液的pH=0
B.a=3
C.阳极生成1.5 mol Cl2
D.阴极析出的金属是铜与铝
下列说法正确的是 ( )。
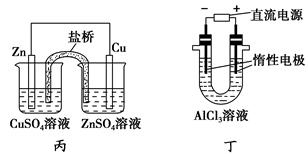
| A.用甲装置电解精炼镁 |
| B.用乙装置验证试管中铁丝发生析氢腐蚀 |
| C.用丙装置构成铜锌原电池 |
| D.用丁装置利用电冶金法制铝 |
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是 ( )。
| A.该过程是将太阳能转化为化学能的过程 |
| B.催化剂a表面发生氧化反应,有O2产生 |
| C.催化剂a附近酸性减弱,催化剂b附近酸性增强 |
| D.催化剂b表面的反应是CO2+2H++2e-=HCOOH |
用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示。则下列说法正确的是 ( )。
| A.构成原电池时b极反应为Cu-2e-=Cu2+ |
| B.构成电解池时a极质量一定减少 |
| C.构成电解池时b极质量可能减少也可能增加 |
| D.构成的原电池或电解池工作后可能产生大量气体 |
下列有关电池的说法不正确的是 ( )。
| A.手机上用的锂离子电池属于二次电池 |
| B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
| C.甲醇燃料电池可把化学能转化为电能 |
| D.锌锰干电池中,锌电极是负极 |
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如下图所示,则下列有关说法中不正确的是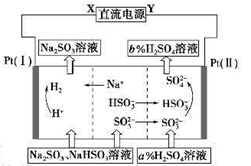
| A.X为直流电源的负极,Y为直流电源的正极 |
| B.阳极区pH增大 |
| C.图中的b>a |
| D.该过程中的产品主要为H2SO4和H2 |
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示,下列说法正确的是( )
| A.电池放电时,Na+从b极区移向a极区 |
| B.电极a采用MnO2,放电时它被还原 |
| C.该电池负极的电极反应式为BH4-+8OH--8e-=BO2-+6H2O |
| D.放电时,a极区溶液的pH升高,b极区溶液pH降低 |
图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色色斑向d端扩散。下列判断正确的是( )
| A.滤纸上c点附近会变红色 |
| B.Cu电极质量减小,Pt电极质量增大 |
| C.烧杯中溶液的pH先减小,后增大 |
| D.烧杯溶液中SO42-向Cu电极定向移动 |