下图是一套电化学装置,对其有关说法错误的是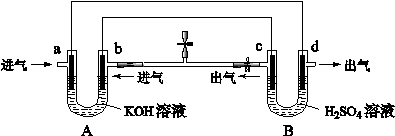
| A.装置A是原电池,装置B是电解池 |
| B.反应一段时间后,装置B中溶液PH增大 |
| C.a口若消耗1mol CH4,d口可产生4mol气体 |
| D.a口通入C2H6时的电极反应为 C2H6 -14e- + 18OH- = 2CO32- + 12H2O |
下列与金属腐蚀有关的说法正确的是
| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
| D.图d中,Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
在铁制品上镀一定厚度的锌层,以下方案设计正确的是( )。
| A.锌作阳极,铁制品作阴极,溶液中含有锌离子 |
| B.铂作阴极,铁制品作阳极,溶液中含有锌离子 |
| C.铁作阳极,铁制品作阴极,溶液中含有亚铁离子 |
| D.锌作阴极,铁制品作阳极,溶液中含有亚铁离子 |
某同学按如图所示的装置进行电解实验。下列说法正确的是( )。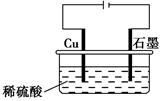
| A.电解过程中,铜电极上有H2产生 |
B.电解初期,主反应方程式为Cu+H2SO4 CuSO4+H2↑ CuSO4+H2↑ |
| C.电解一定时间后,石墨电极上有铜析出 |
| D.整个电解过程中,H+的浓度不断增大 |
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为4Al+3O2+6H2O=4Al(OH)3,下列说法不正确的是( )。
| A.正极反应式为O2+2H2O+4e-=4OH- |
| B.电池工作时,电流由铝电极沿导线流向铂电极 |
| C.以网状的铂为正极,可增大与氧气的接触面积 |
| D.该电池通常只需更换铝板就可继续使用 |
如图所示的装置中铁棒上析出铜,而铁的质量不变,符合要求的原电池是
| A.铁棒作负极,铜棒作正极,电解质溶液是CuSO4溶液 |
| B.镁棒作负极,铁棒作正极,电解质溶液是CuSO4溶液 |
| C.镁棒作负极,铁棒作正极,电解质溶液是FeCl3溶液 |
| D.铁棒作负极,铜棒作正极,电解质溶液是H2SO4溶液 |
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,下列叙述正确的是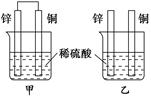
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 |
| D.产生气泡的速率甲比乙慢 |
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是
| A.杠杆为导体或绝缘体时,均为A端高B端低 |
| B.杠杆为导体或绝缘体时,均为A端低B端高 |
| C.当杠杆为导体时,A端低B端高;杠杆为绝缘体时,A端高B端低 |
| D.当杠杆为导体时,A端高B端低;杠杆为绝缘体时,A端低B端高 |
如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当两装置电路中通过的电子都是1 mol时,下列说法不正确的是 ( )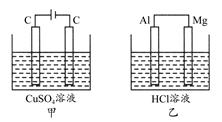
| A.溶液的质量变化:甲减小乙增大 |
| B.溶液pH变化:甲减小乙增大 |
| C.相同条件下产生气体的体积:V甲=V乙 |
| D.电极反应式:甲中阴极为Cu2++2e-=Cu,乙中负极为Mg-2e-=Mg2+ |
蝇类昆虫的雌性信息素可用芥酸(来自白芥)与羧酸X在浓NaOH溶液中进行阳极氧化得到。电解总反应式为
C21H41COOH芥酸+X+4NaOH―→C23H46(雌性信息素)+2Na2CO3+2H2O+H2↑
则下列说法正确的是 ( )
| A.X为C3H7COOH |
| B.电解的阳极反应式为C21H41COOH+X-2e-+2H2O=C23H46+CO32—+6H+ |
| C.电解过程中阴极区pH增大,Na+向阴极移动 |
| D.阴极的还原产物为H2和OH- |