25℃时,弱酸的电离平衡常数如下表,下列表述错误的是
| 弱酸 | CH3COOH | HCN | H2CO3 |
| K | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
A.CN-+H2O+CO2→HCN+HCO3-
B.相同温度时三种溶液的pH关系:Na2CO3> NaCN > CH3COONa
C.等体积、等物质的量浓度的CH3COOH和Na2CO3反应后的溶液呈碱性
D.amol/L HCN与bmol/L NaOH等体积混合溶液c(Na+)>c(CN-),则a一定小于b
常温下,向20.00mL 0.1000 mol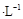 (NH4)2 SO4溶液中逐滴加入0.2000 mol
(NH4)2 SO4溶液中逐滴加入0.2000 mol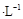 NaOH时,溶液的pH与所加NaOH溶液体积的关系如下图所示(不考虑挥发)。
NaOH时,溶液的pH与所加NaOH溶液体积的关系如下图所示(不考虑挥发)。
下列说法正确的是
| A.点a所示溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| B.点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-) |
| C.点c所示溶液中:c(SO42)+ c(H+)= c(NH3·H2O )+ c(OH-) |
| D.点d所示溶液中:c(SO42)>c(NH3·H2O )>c(OH-)>c(NH4+) |
一定温度下,满足下列条件的溶液一定呈酸性的是
A.pH 的某物质的水溶液 的某物质的水溶液 | B.加酚酞后显无色的溶液 |
| C.能与金属Al反应放出H2的溶液 | D. 的任意物质的水溶液 的任意物质的水溶液 |
室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是
| A.溶液中导电粒子的数目减少 |
B.溶液中 不变 不变 |
| C.醋酸的电离程度增大,c(H+)亦增大 |
| D.再加入10 mL pH=11的NaOH溶液,混合液pH <7 |
室温下,对于0.10 mol·L-1的氨水,下列判断正确的是
| A.与AlCl3溶液反应发生的离子方程式为 Al3++3OH-→Al(OH-)3↓ |
| B.加水稀释后,溶液中c(NH4+)·c(OH-)变大 |
| C.用HNO3溶液完全中和后,溶液不显中性 |
| D.其溶液的pH=13 |
下列说法正确的是
| A.电解质溶液能导电,是因为在通电时电解质电离产生了自由移动的离子 |
| B.饱和石灰水中加入少量CaO,恢复至室温后溶液的pH值不变 |
| C.将AlCl3溶液和Na2SO3溶液分别蒸干并灼烧,得到Al2O3和Na2SO3 |
| D.pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液,则溶液浓度大小关系: |
已知AgI为黄色沉淀,AgCl为白色沉淀.25℃时,AgI饱和溶液中c(Ag+)=1.22×10-8mol·L-1, AgCl饱和溶液中c(Ag+)=1.30×10-5mol·L-1.若在5ml含有KCl和KI浓度均为0.01 mol· L-1的混合溶液中,滴加8ml0.01 mol·L-1的AgNO3溶液,则下列叙述中不正确的是
| A.溶液中所含溶质的离子浓度大小关系为 c(NO3-)>c(K+)> C(Cl-)> c(I-)> c(Ag+) |
| B.溶液中先产生的是AgI沉淀 |
| C.AgCl的Ksp的数值为1.69×10-10 |
| D.若在AgI悬浊液中滴加KCl溶液,黄色沉淀可能转变成白色沉淀 |
下列叙述正确的是( )
| A.pH=5.2的CH3COOH与CH3COONa混合溶液中,c(Na+) > c(CH3COO-) |
| B.在滴有酚酞溶液的氨水里,加入盐酸至溶液恰好无色,则此时溶液的pH=7 |
| C.若100mLpH=11的NaOH溶液与10mL盐酸混合后溶液的pH=7,则盐酸溶液的pH=2 |
| D.某醋酸溶液的pH=3,将此溶液稀释10倍后溶液的pH=4 |
测定CuSO4?nH2O的结晶水含量,方法是:称量样品→ 在坩埚中加热→ 冷却→ 称量无水盐。若用相同方法测试下列晶体中的结晶水含量,可行的是
| A.Cu(NO3)2?nH2O | B.MgCl2?nH2O | C.MgSO4?nH2O | D.FeSO4?nH2O |