25°C时,弱酸的电离平衡常数如下表:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| Ka | 1.8×10-5 | 4.9×10-10 | K1:4.3×10-7 K2:5.6×10-11 |
下列有关说法正确的是( )
A.等物质的量浓度的各溶液的pH关系为:
pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.a mol·L-1HCN与b mol·L-1 NaOH溶液等体积混合后所得溶液中c(Na+)>c(CN-),则a一定小于b
C.往冰醋酸中逐滴加水,溶液导电能力增大
D.NaHCO3和Na2CO3的混合液中:c(Na+)+c(H+)=c(OH-)+c(HCO3—)+2c(CO32—)
为了使FeCl3溶液中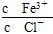 增大,可加入的物质是( )
增大,可加入的物质是( )
| A.适量的HCl气体 | B.适量的硫酸氢钠 |
| C.适量的NaOH固体 | D.适量的NaHCO3溶液 |
常温下,将a L 0.1 mol·L-1的NaOH溶液与b L 0.1 mol·L-1的CH3COOH溶液混合,下列有关混合溶液的说法一定不正确的是( )
| A.a<b时,c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| B.a>b时,c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| C.a=b时,c(CH3COOH)+c(H+)=c(OH-) |
| D.无论a、b有何关系,均有c(H+)+c(Na+)=c(CH3COO-)+c(OH-) |
酸式盐NaHY的水溶液中,HY-的电离程度小于HY-的水解程度。下列有关叙述正确的是 ( )
A.HY-水解方程式为:HY-+ H2O H3O++ Y2- H3O++ Y2- |
| B.在该盐的溶液中离子浓度大小关系为:c(Na+) >c(Y2-) >c(HY-) >c(OH-) >c(H+) |
C.H2Y的电离方程式为:H2Y+H2O HY-+H3O+ HY-+H3O+ |
| D.在该盐的溶液中:c(Na+) >c(HY-) >c(Y2-)>c(OH-)>c(H+) |
现有两正盐的稀溶液,分别是a mol·L-1NaX溶液和b mol·L-1NaY溶液。下列说法不正确的是 ( )
| A.若a>b,测得c(X-)=c(Y-),可推出溶液中的c(HX)>c(HY) |
| B.若a>b,测得c(X-)=c(Y-),可推可溶液中的c(HX)=c(HY) |
| C.若a=b,且pH(NaX溶液)>pH(NaY溶液),则相同浓度时,酸性HX<HY |
| D.若a=b,并测得a=c(X-)=c(Y-)+c(HY),则HX是强酸,HY是弱酸 |
下列关于电解质溶液的叙述正确的是( )
| A.常温下,在pH=7的醋酸钠和醋酸混合溶液中:c(CH3COO-)>c(Na+) |
| B.稀释醋酸溶液,溶液中所有离子的浓度均降低 |
| C.在pH=5的氯化钠和稀硝酸的混合溶液中,c(Na+)=c(Cl-) |
| D.0.1 mol·L-1的硫化钠溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) |
等物质的量浓度、等体积的下列溶液中:
①H2CO3、②Na2CO3、③NaHCO3、④NH4HCO3、⑤(NH4)2CO3,下列关系或者说法正确的是( )
| A.c(CO32—)的大小关系为:②>⑤>③>④>① |
| B.c(HCO3—)的大小关系为:④>③>⑤>②>① |
| C.将溶液蒸干灼烧后只有①不能得到对应的固体物质 |
| D.②③④⑤既能与盐酸反应,又能与NaOH溶液反应 |
下列反应不属于水解反应或水解方程式不正确的是 ( )
①HCl+H2O H3O++Cl-
H3O++Cl-
②AlCl3+3H2O=Al(OH)3+3HCl
③Na2CO3+2H2O H2CO3+2NaOH
H2CO3+2NaOH
④碳酸氢钠溶液:HCO3—+H2O CO32—+H3O+
CO32—+H3O+
⑤NH4Cl溶于D2O中:NH4++D2O NH3·D2O+H+
NH3·D2O+H+
| A.①②③④ | B.①②③ | C.②③⑤ | D.全部 |
下列说法中正确的是 ( )
| A.饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH增大 |
B.AgCl悬浊液中存在平衡:AgCl(s) Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 |
| C.AgCl悬浊液中加入KI溶液,白色沉淀变成黄色,证明此条件下Ksp(AgCl)>Ksp(AgI) |
| D.硬水中含有较多的 Ca2+、Mg2+、HCO3—、SO42—,加热煮沸可以完全除去其中的Ca2+、Mg2+ |
已知如下物质的溶度积常数:FeS,Ksp=6.3×10-18;CuS,Ksp=1.3×10-36;ZnS,Ksp=1.6×10-24。下列说法正确的是 ( )
| A.同温度下,CuS的溶解度大于ZnS的溶解度 |
| B.将足量CuSO4溶解在0.1 mol·L-1的H2S溶液中,Cu2+能达到的最大浓度为1.3×10-35mol·L-1 |
| C.因为H2SO4是强酸,所以Cu2++H2S=CuS↓+2H+不能发生 |
| D.除去工业废水中的Cu2+,可以选用FeS作沉淀剂 |