下列依据热化学方程式得出的结论正确的是( )
| A.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ・mol-1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量 |
| B.已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ・mol--1,则氢气的燃烧热为241.8 kJ・mol-1 |
| C.已知2C(s)+2O2(g)=2CO2(g)△H=a、2C(s)+O2(g)=2CO(g)△H=b,则a>b |
| D.已知P (白磷,s)=P (红磷,s)△H<0,则白磷比红磷稳定 |
下列热化学方程式正确的是( )
A.2SO2+O2 2SO3 ΔH=-196.6 kJ・mol-1 2SO3 ΔH=-196.6 kJ・mol-1 |
| B.C(g)+O2(g)=CO(g) ΔH=393.5 kJ・mol-1 |
C.H2(g)+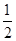 O2(g)=H2O(g) ΔH=-241.8 kJ O2(g)=H2O(g) ΔH=-241.8 kJ |
| D.2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ・mol-1 |
已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,判断下列叙述中正确的是( )
| A.每生成2分子AB吸收b kJ热量 |
| B.该反应热ΔH=+(a-b)kJ・mol-1 |
| C.该反应中反应物的总能量高于生成物的总能量 |
| D.断裂1 mol A―A和1 mol B―B键,放出a kJ能量 |
为了测定中和反应的反应热,计算时至少需要的数据是( )
①酸的浓度和体积 ②碱的浓度和体积 ③比热容④反应后溶液的质量
⑤生成水的物质的量 ⑥反应前后溶液温度变化 ⑦操作所需的时间
| A.①②③⑥ | B.①③④⑥ |
| C.③④⑤⑥ | D.全部 |
下列与化学反应能量变化相关的叙述正确的是( )
| A.生成物能量一定低于反应物总能量 |
| B.放热反应不必加热就一定能发生 |
| C.应用盖斯定律,可计算某些难以直接测量的反应的焓变 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的ΔH不同 |
[双选题]下列反应属于放热反应的是( )
| A.锌粒与稀H2SO4反应 | B.NaOH溶于水 |
| C.KClO3受热分解 | D.CaO溶于水 |
以NA代表阿伏加德罗常数,则关于热化学方程式C2H2(g)+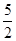 O2(g)=2CO2(g)+H2O(l) ΔH=-1300 kJ/mol 的说法中,正确的是( )
O2(g)=2CO2(g)+H2O(l) ΔH=-1300 kJ/mol 的说法中,正确的是( )
| A.当转移10NA个电子时,该反应放出1300 kJ的能量 |
| B.当1NA个水分子生成且为液体时,吸收1300 kJ的能量 |
| C.当2NA个碳氧共用电子对生成时,放出1300 kJ的能量 |
| D.当8NA个碳氧共用电子对生成时,放出1300 kJ的能量 |
含1 mol Ba(OH)2的稀溶液与足量稀盐酸反应,放出热量114.6 kJ。下列热化学方程式中正确的是( )
| A.Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(l) ΔH=+114.6 kJ/mol |
| B.Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(l) ΔH=-114.6 kJ/mol |
C. Ba(OH)2(aq)+HCl(aq)= Ba(OH)2(aq)+HCl(aq)= BaCl2(aq)+H2O(l) ΔH=-57.3 kJ/mol BaCl2(aq)+H2O(l) ΔH=-57.3 kJ/mol |
D. Ba(OH)2(aq)+HCl(aq)= Ba(OH)2(aq)+HCl(aq)= BaCl2(aq)+H2O(l) ΔH=+57.3 kJ/mol BaCl2(aq)+H2O(l) ΔH=+57.3 kJ/mol |
常温下,已知:
4Al(s)+3O2(g)=2Al2O3(s)ΔH1
4Fe(s)+3O2(g)=2Fe2O3(s)ΔH2
下面关于ΔH1、ΔH2的比较正确的是( )
| A.ΔH1>ΔH2 | B.ΔH1<ΔH2 |
| C.ΔH1=ΔH2 | D.无法计算 |
火电厂利用燃煤发电,煤燃烧中的热化学方程式有:
C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
CO(g)+ O2(g)=CO2(g)ΔH2=-283 kJ/mol
O2(g)=CO2(g)ΔH2=-283 kJ/mol
C(s)+ O2(g)=CO(g)ΔH3=?
O2(g)=CO(g)ΔH3=?
下列有关说法中不正确的是( )
| A.CO的燃烧热为283 kJ/mol |
| B.二氧化碳分解为一氧化碳和氧气的反应是吸热反应 |
| C.ΔH3=ΔH2-ΔH1=110.5 kJ/mol |
| D.ΔH3=ΔH1-ΔH2=-110.5 kJ/mol |