关于晶体的叙述中,正确的是
| A.原子晶体中,共价键的键能越大,熔、沸点越高 |
| B.分子晶体中,分子间的作用力越大,该分子越稳定 |
| C.分子晶体中,共价键的键能越大,熔、沸点越高 |
| D.某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体 |
下列说法正确的是
| A.已知Ag2CrO4的Ksp为1.12×10-12,则将等体积的1×10-3mo1/L的AgNO3溶液和1×0-3mo1/LK2CrO4溶液混合,会有Ag2CrO4沉淀产生 |
| B.Si—O键的键能大于Si—Cl键的键能,因此SiO2的熔点高于晶体SiCl4的熔点 |
| C.常温时,浓度均为0.01mol/L Na2CO3溶液和NaHCO3溶液,等体积混合,其溶液中粒子浓度关系为3c(Na+)=2c(HCO3-)+2c(CO32-)+2c(H2CO3) |
| D.已知:2CO(g)+O2(g)=2CO2(g) △H=-566kJ·mol-1,下图可表示由CO生成CO2的反应过程和能量关系 |

由碳原子构成的纳米碳管可以作为储存氢气的优良容器,其单层部分结构示意图如下,下列说法正确的是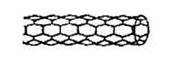
| A.纳米碳管是一种无机化合物 |
| B.纳米碳管中碳原子间以共价键结合 |
| C.纳米碳管与石墨互为同位素 |
| D.0.12g纳米碳管中含有6.02×l022个碳原子 |
NaCl的晶胞如图所示,将NaCl晶胞中的所有Cl-去掉,并将Na+全部换成C原子,再在晶胞的4个“小立方体”中心处各放置一个C原子,且这四个“小立方体”互不共面,位于“小立方体”中的碳原子均与最近的4个碳原子成键,以此表示金刚石的一个晶胞。若再将在成键的C原子中心联线的中点处增添一个O原子,则构成了某种CO2的晶胞。则下面说法正确的是( )(已知C-C键的键长1.54×10-10m)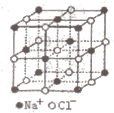
| A.一个金刚石的晶胞中有8个C原子 |
| B.金刚石的密度为3.54g·cm-1 |
| C.在该种CO2晶体中,一个CO2分子由一个C原子和二个氧原子构成 |
| D.在该种CO2晶胞中含氧原子8个 |
水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165K(零下108℃)时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是( )
| A.水由液态变为玻璃态,体积缩小 |
| B.玻璃态水变成冰发生化学变化 |
| C.玻璃态是水的一种特殊状态 |
| D.玻璃态水与冰的化学性质不同 |
有关A1型密堆积与A3型密堆积的说法中正确的是( )。
| A.A1型密堆积是最密堆积,A3型密堆积不是最密堆积 |
| B.两者都是最密堆积,其中A3型密堆积是一、三、五……各层球心重合,二、四、六……各层球心重合;A1型密堆积是四、五、六各层球心分别和一、二、三各层球心重合 |
| C.原子晶体一般都采用A1型密堆积或A3型密堆积 |
| D.只有金属晶体才可能采用A1型密堆积或A3型密堆积 |
将晶体划分为离子晶体、金属晶体、原子晶体和分子晶体的本质标准是( )。
| A.基本构成微粒种类 |
| B.晶体中最小重复结构单元的种类 |
| C.微观粒子的密堆积种类 |
| D.晶体内部微粒的种类及微粒间相互作用的种类 |
下列晶体按A1型方式进行紧密堆积的是( )。
| A.干冰、NaCl、金属铜 |
| B.ZnS、金属镁、氮化硼 |
| C.水晶、金刚石、晶体硅 |
| D.ZnS、NaCl、金属镁 |
关于晶体的自范性,下列叙述正确的是( )。
| A.破损的晶体能够在固态时自动变成规则的多面体 |
| B.缺角的氯化钠晶体在饱和的NaCl溶液中慢慢变为完美的立方块 |
| C.圆形容器中结出的冰是圆形的 |
| D.由玻璃制成的圆形的玻璃球 |
水的状态除了气、液和固态外,还有玻璃态,它是由液态水急速冷却到165 K时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同。有关玻璃态水的叙述正确的是( )。
| A.水由液态变为玻璃态,体积缩小 |
| B.水由液态变为玻璃态,体积膨胀 |
| C.玻璃态是水的一种特殊状态 |
| D.玻璃态水是分子晶体 |