下列化合物按其晶体的熔点由高到低排列正确的是( )。
| A.SiO2 CsCl CBr4 CF4 |
| B.SiO2 CsCl CF4 CBr4 |
| C.CsCl SiO2 CBr4 CF4 |
| D.CF4 CBr4 CsCl SiO2 |
下列有关分子晶体熔点的高低叙述中,正确的是( )。
| A.Cl2>I2 | B.SiCl4>CCl4 |
| C.N2>O2 | D.C(CH3)4>CH3CH2CH2CH2CH3 |
下列性质适合于分子晶体的是( )。
| A.熔点1 070 ℃,易溶于水,水溶液能导电 |
| B.熔点10.31 ℃,液态不导电,水溶液导电 |
| C.难溶于CS2,熔点1 128 ℃,沸点4 446 ℃ |
| D.熔点97.81 ℃,质软导电,密度0.97 g·cm-3 |
下列晶体中由原子直接构成的单质有( )。
| A.硫 | B.生铁 | C.金刚石 | D.金属镁 |
下表是某些原子晶体的熔点和硬度
| 原子晶体 | 金刚石 | 氮化硼 | 碳化硅 | 石英 | 硅 | 锗 |
| 熔点/℃ | 3 900 | 3 000 | 2 700 | 1 710 | 1 410 | 1 211 |
| 硬度 | 10 | 9.5 | 9.5 | 7 | 6.5 | 6.0 |
分析表中的数据,判断下列叙述正确的是( )。
①构成原子晶体的原子种类越多,晶体的熔点越高
②构成原子晶体的原子间的共价键键能越大,晶体的熔点越高
③构成原子晶体的原子的半径越大,晶体的硬度越大
④构成原子晶体的原子的半径越小,晶体的硬度越大
A.①② B.③④ C.①③ D.②④
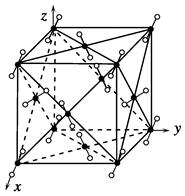
氢是重要而洁净的能源。要利用氢气作为能源,必须解决好安全有效地储存氢气的问题。化学家研究出利用合金储存氢气的方法,其中镧(La)镍(Ni)合金是一种储氢材料,这种合金的晶体结构已经测定,其基本结构单元如图所示,则该合金的化学式可表示为( )。
| A.LaNi5 | B.LaNi | C.La14Ni24 | D.La7Ni12 |
下列对化学知识概括合理的是( )。
| A.原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键 |
| B.同素异形体之间的转化都是物理变化 |
| C.原子晶体的熔点不一定比金属晶体的高,分子晶体的熔点不一定比金属晶体的低 |
| D.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物 |
下列各类物质中,固态时只能形成离子晶体的是( )。
| A.非金属氧化物 | B.非金属单质 | C.强酸 | D.强碱 |
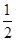 ,n=3、l=1、m=0、ms=+
,n=3、l=1、m=0、ms=+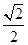 a(其中a为立方体棱长)的CO2有( )。
a(其中a为立方体棱长)的CO2有( )。