X、Y、Z、W、M五种元素的原子序数依次增大。已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的阴离子核外电子排布与氦原子相同,Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍,M是地壳中含量最高的金属元素。下列说法中正确的是( )
| A.五种元素的原子半径从大到小的顺序是:M>W>Z>Y>X |
| B.化合物X2W2、YW2、ZW2等都含有极性共价键和非极性共价键 |
| C.用M单质作阳极,石墨电极作阴极电解NaHCO3溶液,电解一段时间后,在阴极区会出现白色沉淀 |
| D.X、Z两元素能形成原子个数比为3∶1和4∶2的化合物 |
下图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是( )
| A.Z、N两种元素的离子半径相比,前者较大 |
| B.X、M两种元素的气态氢化物的稳定性相比,前者较弱 |
| C.由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应 |
| D.Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液 |
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A.原子半径A>B>C>D |
| B.原子序数a>b>c>d |
| C.离子半径C3->D->B+>A2+ |
| D.单质的还原性A>B>D>C |
下列关于元素性质和结构的递变情况的说法错误的是( )
| A.Li、Be、B原子最外层电子数依次增多 |
| B.P、S、Cl元素最高正价依次升高 |
| C.N、O、F原子半径依次增大 |
| D.Na、K、Rb的电子层数逐渐增多 |
同一主族的两种元素的原子序数之差不可能是( )
| A.16 | B.26 | C.36 | D.46 |
第三周期主族元素R,它的原子最外电子层上达到饱和所需电子数小于次外层和最内层电子数之差,但等于最内层电子数的正整数倍。下列说法正确的是( )
| A.常温下,能稳定存在的R的氧化物都能与烧碱溶液反应 |
| B.在常温下,R的气态氢化物都能在空气中稳定存在 |
| C.在固态时,R的单质都不与NaOH溶液反应 |
| D.R的最高价氧化物对应的水化物都是强酸 |
X和Y属短周期元素,X原子的最外层电子数是次外层的2倍,Y位于X的前一周期,且最外层只有一个电子,则X和Y形成的化合物的分子式可表示为( )
| A.XY | B.XY2 | C.Y3X | D.XY4 |
随着科学技术的不断进步,研究物质的手段和途径越来越多,H3、O4、C60、N5+等已被发现。下列有关说法中,正确的是( )
| A.H2与H3属于同素异形体 |
| B.O2与O4属于同位素 |
| C.C60的质量数为 720 g/mol |
| D.N5+中含有36个电子 |
下图是某短周期元素最高价氧化物对应水化物相同浓度稀溶液的pH与原子半径的关系示意图,则下列说法正确的是(双选) ( )。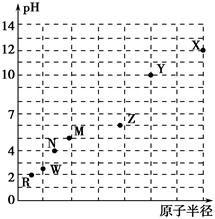
| A.原子序数:W>Z>X |
| B.气态氢化物的稳定性:N>R |
| C.Y和W形成共价化合物 |
| D.X、Z的最高价氧化物对应的水化物能相互反应 |