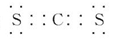X、Y均为短周期元素,X位于ⅠA族,X、Y能形成X2Y型化合物,下列说法中正确的是( )
| A.X与Y形成的化合物中原子个数比可能为1∶1 |
| B.X2Y不可能是共价化合物 |
| C.X和Y分别形成的简单离子不可能具有相同电子层结构 |
| D.根据周期表递变规律判断X原子半径一定大于Y原子半径 |
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | W |
| 原子半径/10-12 m | 160 | 110 | 70 | 66 |
| 主要化合价 | +2 | +5、+3、-3 | +5、+3、-3 | -2 |
下列叙述正确的是 ( )。
A.离子半径:W<X
B.气态氢化物的稳定性:Z>W
C.化合物X3Z2中既含有离子键又含有共价键
D.最高价氧化物对应水化物的酸性:Z>Y
下列有关元素的性质及其递变规律正确的是 ( )。
| A.ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 |
| B.第二周期元素从左到右,最高正价从+1递增到+7 |
| C.同主族元素的简单阴离子还原性越强,水解程度越大 |
| D.同周期金属元素的化合价越高,其原子失电子能力越强 |
X、Y是元素周期表中ⅦA族的两种元素,下列能说明X的非金属性比Y强的是 ( )。
| A.电子层数:X>Y |
| B.气态氢化物的稳定性:HX<HY |
| C.酸性:HXO4>HYO4 |
| D.能发生置换反应:Y2+2NaX=X2+2NaY |
短周期元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为14。X与Z同主族,Y与W同主族,且X的原子半径小于Y。下列叙述正确的是( )。
| A.Y的简单阴离子半径小于Z的简单阳离子半径 |
| B.Y与X形成的化合物沸点高于W与X形成的化合物的沸点 |
| C.X2Y2加入酸性高锰酸钾溶液中,X2Y2作氧化剂 |
| D.W元素的最高价氧化物对应的水化物是弱酸 |
V、W、X、Y均是元素周期表中短周期元素,在周期表中的相对位置关系如表所示:
| | Y | V | | |
| X | | | | W |
Z为第四周期常见元素,该元素是人体血液中血红蛋白最重要的组成金属元素。V的最简单氢化物为甲,W的最简单氢化物为乙,甲、乙混合时有白烟生成。下列说法正确的是( )。
A.原子半径:X>Y>V>W
B.X、W的质子数之和与最外层电子数之和的比值为2∶1
C.甲、乙混合时所生成的白烟为离子化合物,但其中含有共价键
D.少量Z的单质与过量W的单质可化合生成ZW2
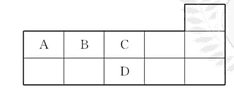
X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如图所示。若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )。
| A.只由这四种元素不能组成有机化合物 |
| B.最高价氧化物对应的水化物的酸性W比Z弱 |
| C.Z的单质与氢气反应较Y剧烈 |
| D.X、Y形成的化合物都易溶于水 |