已知X、Y均为1~18号之间的元素,X、Y可形成化合物X2Y和X2Y2,又知Y的原子序数小于X的原子序数,则两种元素的原子序数之和为( )。
| A.19 | B.18 | C.27 | D.9 |
(双选)原子序数从11依次增加到17,下列递变关系错误的是( )。
| A.电子层数逐渐增多 |
| B.原子半径逐渐增大 |
| C.最高正价数值逐渐增大 |
| D.从硅到氯,负价从-4到-1 |
下列说法正确的是( )。
| A.NaCl固体中含有共价键 |
| B.CO2分子中含有离子键 |
C. C是碳元素的三种核素 C是碳元素的三种核素 |
D.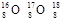 O含有相同的中子数 O含有相同的中子数 |
(双选)短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是( )。
| A.元素X的简单气态氢化物的热稳定性比W的强 |
| B.元素W的最高价氧化物对应水化物的酸性比Z的弱 |
| C.化合物YX、ZX2、WX3中化学键的类型相同 |
| D.原子半径的大小顺序:rY>rZ>rW>rX |
有人建议将氢元素排在元素周期表的第ⅦA族。下列事实能支持这一观点的是( )。
①氢原子得到一个电子后最外层电子达到稳定结构 ②氢分子的结构式为H—H ③与碱金属元素形成离子化合物M+[∶H]- ④分子中原子间的化学键都属于非极性键
| A.①②③ | B.①③④ | C.②③④ | D.①②③④ |
元素周期表在指导科学研究和生产实践方面具有十分重要的意义,请将下表中A、B两栏描述的内容对应起来。
| A | B | A | B |
| ①制半导体的元素 | (a)ⅢB至ⅥB的过渡元素 | ① | |
| ②制催化剂的元素 | (b)F、Cl、Br、N、S“三角地带” | ② | |
| ③制耐高温材料的元素 | (c)金属与非金属元素分界线附近 | ③ | |
| ④制制冷剂的元素 | (d)相对原子质量较小的元素 | ④ | |
| ⑤地壳中含量较多的元素 | (e)过渡元素 | ⑤ | |
第二周期元素R,它的最外电子层达到稳定结构所需电子数小于最外层达到稳定结构时的电子数和最内层电子数之差,并且等于最内层电子数的整数倍。则关于R的正确说法是( )。
| A.常温下能稳定存在的R的氧化物都能和烧碱溶液起反应 |
| B.R最高价氧化物对应水化物都是强酸 |
| C.R的最简单氢化物可能有两种,其稳定性一种比NH3强,另一种比NH3弱 |
| D.R的最简单氢化物受热时都易分解 |
(双选)某元素X的原子序数为52,下列叙述正确的是( )。
| A.X的主要化合价是-2、+4、+6 |
| B.X可以形成稳定的气态氢化物 |
| C.X的最高价氧化物对应水化物的酸性比HBrO4的酸性强 |
| D.X的简单阴离子的还原性比溴离子强 |