短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍。下列判断正确的是( )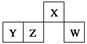
| A.原子半径:rW>rZ>rY>rX |
| B.含Y元素的盐溶液显酸性 |
| C.最简单气态氢化物的热稳定性:Z>W |
| D.X与氢元素组成的化合物XH5与水反应可产生两种气体 |
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性R>W |
| C.WX3和水反应形成的化合物是离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
下列实验不能达到预期目的的是( )
| 序号 | 实验操作 | 实验目的 |
| A | Cl2、Br2分别与H2反应 | 比较氯、溴的非金属性强弱 |
| B | MgCl2、AlCl3溶液中分别通入NH3 | 比较镁、铝的金属性强弱 |
| C | 测定同浓度的Na2CO3、Na2SO4溶液的pH | 比较碳、硫的非金属性强弱 |
| D | Fe、Cu分别与盐酸反应 | 比较铁、铜的金属性强弱 |
已知X、Y、Z都是短周期元素,它们的原子序数依次增大,X原子的电子层数与它的核外电子总数相等,而Z原子的最外层电子数是次外层的3倍,Y和Z可以形成两种以上气态化合物,则下列说法错误的是( )
| A.Y和Z可以组成一种Y和Z的质量比为7∶8的化合物 |
| B.X、Y、Z可以组成一种盐 |
| C.X和Z可以组成原子个数比分别为1∶1和2∶1常温下呈液态的两种化合物 |
| D.由X、Y、Z三种元素中的任意两种组成的10电子微粒有2种 |
原子的核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数为2n2-1。下列有关X的说法中不正确的是( )
| A.X能形成化学式为X(OH)3的碱 |
| B.X能与某些金属元素形成化合物 |
| C.X原子的最外层电子数和核电荷数肯定为奇数 |
| D.X可能形成化学式为KXO3的盐 |
X、Y、Z均为短周期元素。已知X元素的某种原子核内无中子,Y元素的原子核外最外层电子数是其次外层电子数的2倍,Z元素是地壳中含量最丰富的元素。有下列含这三种元素的化学式:
①X2Y2Z2;②X2YZ3;③X2YZ2;④X2Y2Z4;⑤X3YZ4;⑥XYZ3,其中可能存在的是( )
| A.② | B.②④⑤ | C.②⑤⑥ | D.①②③④ |
从宏观方面看物质是由元素组成的,从微观方面看物质是由粒子构成的,下列有关说法不正确的是( )
| A.元素原子的多样性是由构成原子的质子和中子数目引起的 |
| B.元素的化学性质主要取决于元素原子的最外层电子数 |
| C.只由一种分子构成的物质一定是纯净物 |
| D.质子数等于电子数的微粒,可能是一种分子和一种离子 |
已知X为第三周期元素的原子,该原子要达到8电子稳定结构,则需要的电子数小于其次外层和最内层的电子数之差,且等于最内层电子数的整数倍。下列说法正确的是( )
| A.X元素最高价氧化物对应的水化物一定是强酸 |
| B.X元素的氢化物的化学式一定为H2X |
| C.X的单质一定是良好的半导体材料 |
| D.X元素的氧化物一定能与烧碱反应 |
对于符号:35Cl和37Cl、H2和D2、1H216O和2H218O。下列有关说法正确的是( )
| A.35Cl和37Cl互称为同素异形体 |
| B.H2和D2是氢元素的两种同位素 |
| C.35和37表示的是质量数 |
| D.1H216O和2H218O表示同一种水分子 |