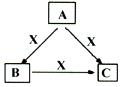
下列有关物质的性质与应用均正确的是
| A.MgO的熔点很高,可用于制作耐高温材料 |
| B.Na2O2是碱性氧化物,具有强氧化性可用于杀菌消毒 |
| C.氨气是一种碱性气体,可用P2O5或无水CaCl2干燥 |
| D.SO2和Cl2都能使品红溶液褪色,两者等体积混合可以增强漂白能力 |
下列根据实验操作和现象所得出的结论不正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2 min后,试管里出现凝胶 | 酸性:盐酸>硅酸 |
| B | 在酒精灯上加热铝箔 | 铝箔熔化但不滴落 | 熔点:氧化铝>铝 |
| C | 常温下,向浓硫酸中投入铁片 | 铁片不溶解 | 常温下,铁不与浓硫酸反应 |
| D | 向某溶液中先滴加KSCN溶液,再滴加少量氯水 | 先无明显现象,后溶液变成血红色 | 溶液中含有Fe2+,没有Fe3+ |
类比推断法是研究物质性质的常用方法之一,可预测许多物质的性质。但类比推断法是相对的,不能违背客观实际。下列说法正确的是
| A.由溶解性CaCO3<Ca(HCO3)2,则溶解性Na2CO3<NaHCO3 |
| B.向Ca(ClO)2溶液中通入少量CO2可得到CaCO3,则向Ca(ClO)2溶液中通入少量SO2可得到CaSO3 |
| C.由O2与Li加热生成Li2O,则O2与Na加热生成Na2O |
| D.有Fe与S加热生成FeS,则Cu与S加热生成Cu2S |
对下列过程中发生反应的叙述正确的是
| A.海水中含有钾元素,只需经过物理变化可以得到钾单质 |
| B.Na+、Mg2+、Al3+得电子能力很弱,故常用电解熔融氯化物的方法来制备其单质 |
| C.从铝土矿中分离出氧化铝的过程中不涉及氧化还原反应 |
| D.从海水中提取溴单质的过程中所涉及的反应均是置换反应 |
下列物质转化在给定条件下不能实现的是
| A.①③⑤ | B.②③④ | C.②③⑤ | D.①④⑤ |
对溶液中的反应,如图图像中m表示生成沉淀的物质的量,n表示参加反应的某一种反应物的物质的量,则下列叙述中错误的是
甲 乙 丙
| A.符合甲图像的两种反应物可以是AlC13和NaOH |
| B.符合乙图像的两种反应物可以是Ca(OH)2和CO2 |
| C.符合丙图像的反应可以是在Ca(OH)2和KOH的混合溶液中通入CO2 |
| D.符合丙图像的反应可以是在NH4Al(SO4)2溶液中加入NaOH |
下列有关实验操作的叙述正确的是
| A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 |
| B.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性 |
| C.NaCl 溶液蒸发结晶时,蒸发皿中刚好有晶体析出时即停止加热 |
| D.向AlCl3溶液中滴加氨水,会产生白色沉淀,再加入NaHSO4溶液,沉淀不消失 |
下列说法中,正确的是
| A.铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜的熔点高于铝 |
| B.向氢氧化铁胶体中加入少量稀硫酸,因发生化学反应而产生红褐色沉淀 |
| C.电子工业用30%的氯化铁溶液腐蚀敷在印刷线路板上的铜箔:Fe3++Cu= Fe2++Cu2+ |
| D.标况下,NA个SO2分子和NA个SO3分子的体积相同(NA表示阿伏加德罗常数值) |
对下列实验的现象描述正确的是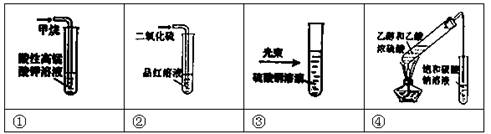
| A.实验①溶液褪色 | B.实验③溶液中看到一条光亮的通路 |
| C.实验②溶液褪色 | D.实验④饱和碳酸钠溶液下方出现油状液体 |