两种盐的固体混合物:①加热时有气体产生,②加水溶解时有沉淀生成,且沉淀溶于稀盐酸。满足上述条件的混合物是
| A.BaCl2和(NH4)2SO4 | B.AgNO3和NH4Cl |
| C.FeCl3和NaHCO3 | D.KCl和Na2CO3 |
类推的思维方法是化学学习和研究中常用的重要思维方法,但所得结论要经过实践的检验才能确定其正确与否。根据你所掌握的知识,判断下列类推结论中正确的是
| | 化学事实 | 类推结论 |
| A | pH=3的盐酸稀释1000倍后pH=6 | pH=6的盐酸稀释1000倍后pH=9 |
| B | 用电解熔融MgCl2的方法冶炼金属镁 | 用电解熔融NaCl的方法冶炼金属钠 |
| C | 将SO2通入BaCl2溶液中无沉淀生成 | 将SO2通入Ba(NO3)2溶液中也无沉淀生成 |
| D | Al在O2中燃烧生成Al2O3 | Fe在O2中燃烧生成Fe2O3 |
下列实验现象与对应结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 常温下将Cu片放入浓H2SO4中 | 生成刺激性气味气体 | Cu与浓H2SO4反应生成SO2 |
| B | Al2(SO4)3溶液中滴加过量氢氧化钡溶液 | 生成白色沉淀 | Al(OH)3不溶于氢氧化钡溶液 |
| C | 向某溶液中加入KSCN溶液,再向溶液中加入新制氯水 | 溶液先不显红色,加入氯水后变红色 | 该溶液中含有Fe2+ |
| D | 向某溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 该溶液中存在I- |
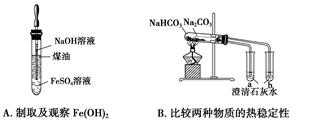
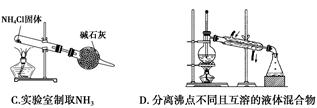
下列有关实验或操作的叙述正确的是( )
| A.用图1所示的装置做喷泉实验时观察到产生白色喷泉 |
| B.如图2所示的两套装置均可制备NH3(不考虑净化和收集) |
| C.称取2.5 g CuSO4·5H2O,放入100 mL容量瓶中,配制0.10 mol·L-1CuSO4溶液 |
| D.除去NaHCO3溶液中的Na2CO3,可加入Ca(OH)2溶液后过滤 |
从下列事实所得出的相应结论正确的是( )
| | 实验事实 | 结论 |
| ① | 在相同温度下,向1 mL 0.2 mol·L-1 NaOH溶 液中滴入2滴0.1 mol·L-1 MgCl2溶液,产生 白色沉淀后,再滴加2滴0.1 mol·L-1 FeCl3 溶液,又生成红褐色沉淀 | 溶解度:Mg(OH)2>Fe(OH)3 |
| ② | 将CO2通入到Na2SiO3溶液中产生白色浑浊 | 酸性:H2CO3>H2SiO3 |
| ③ | 已知反应5Cl2+I2+6H2O=2HIO3+ 10HCl,2BrO+Cl2=2ClO+Br2 | 氧化性强弱顺序:BrO>Cl2>ClO>IO |
| ④ | 测定等物质的量浓度的Na2SO4与Na2CO3溶 液的pH,后者较大 | 非金属性:S>C |
A.③④ B.②④ C.①②③ D.全部
下列说法不正确的是
| A.青铜中含有的主要合金元素是锡和铅 |
| B.装运浓硫酸的铝罐车,在卸货后不能用水冲洗铝罐的内部 |
| C.半导体工业所说的“从沙滩到用户”是指将二氧化硅制成晶体硅 |
| D.氮的固定只有在高温、高压、催化剂的条件下才能实现 |
下列实验的现象与对应结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 将Cl2通入KI溶液 | 溶液变蓝色 | I-的还原性强于Cl- |
| B | 常温下将Fe片放入浓硫酸中 | 无明显变化 | 可以用铁槽车装运浓硫酸 |
| C | 将一小块Na放入硫酸铜溶液中 | 有红固体析出 | Na的活泼性强于铜 |
| D | 向AgCl浊液中滴加Na2S溶液 | 黑色沉淀生成 | Ksp(AgCl)>Ksp(Ag2S) |
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
| 编号 | 叙述I | 叙述II |
| A | MgO和Al2O3的熔点都很高 | Mg(OH)2和Al(OH)3可以作阻燃剂 |
| B | SO2具有漂白性 | SO2能使高锰酸钾酸性溶液褪色 |
| C | AlCl3的熔融态不导电 | AlCl3是弱电解质 |
| D | Fe3+具有氧化性 | Fe3+与KSCN溶液显血红色 |