用如图所示装置进行实验,下列对实验现象的解释不合理的是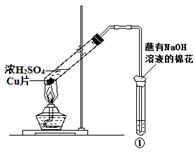
| | ①中试剂 | ①中现象 | 解 释 |
| A | Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成白色BaSO3沉淀 |
| B | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
| C | 紫色石蕊溶液 | 溶液变红 | SO2与水反应生成酸 |
| D | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
已知铜与稀硫酸不发生反应,但如果在铜与稀硫酸的混合溶液中加入某种盐,就能发生反应,且有气体、有沉淀产生,则该盐是
| A.FeCl3 | B.Ba(NO3)2 | C.Na2SO4 | D.KCl |
下列有关双氧水说法错误的是
| A.H2O2、Na2O2都属于过氧化物,都存在共价键 |
| B.双氧水是绿色氧化剂,可作医疗消毒剂 |
| C.H2O2在过氧化氢酶的催化下,温度越高,分解速率越快 |
| D.H2O2做漂白剂是利用其氧化性,漂白原理与HClO类似、与SO2不同 |
NH3是重要的化工原料,可以制备一系列物质(如图所示)。下列说法正确的是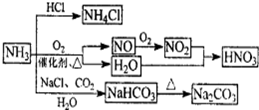
| A.NH4Cl和NaHCO3都是常用的化肥 |
| B.NH4Cl、HNO3和Na2CO3受热时都易分解 |
| C.NH3和NO2在一定条件下可发生氧化还原反应 |
| D.图中所涉及的盐类物质均可以发生水解反应 |
用内置有螺旋状铜丝的胶头滴管小心吸取一滴管浓硝酸后迅速插入细口瓶中(如图),滴管与瓶口接触处垫一小块滤纸使滴管与瓶口留少量空隙,依次观察到如下现象:①滴管内产生红棕色气体,液面下降;②滴管内液面上升,气体变成无色;③滴管内液面再次下降.下列说法中不正确的是
| A.现象①中产生的红棕色气体为NO2 |
| B.产生现象②的原因是NO2与水反应 |
| C.产生现象③的原因是铜与稀硝酸反应 |
| D.最终瓶内溶液中的溶质一定只有Cu(NO3)2 |
“84”消毒液在日常生活中使用广泛。该消毒液无色,有漂白作用。它的有效成分是
A.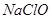 | B.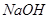 | C.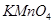 | D.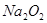 |
在下列用途或反应中,硫酸表现出的性质为:
| A.高沸点性; | B.酸性; | C.吸水性; | D.脱水性;(E)强氧化性。试用字母填空: |
(3)将浓硫酸加到浓盐酸中产生白雾:__________;
(4)浓硫酸可使湿润的蓝色石蕊试纸先变红,后变黑:______________。
下列关于硅单质及其化合物的说法正确的是( )
①硅是构成一些岩石和矿物的基本元素
②水泥、玻璃、水晶饰物都是硅酸盐制品
③高纯度的硅单质广泛用于制作光导纤维
④陶瓷是人类应用很早的硅酸盐材料
| A.①④ | B.②③ | C.①② | D.③④ |
对下列事实的解释正确的是( )
| A.浓硝酸通常保存在棕色的试剂瓶中,说明浓硝酸不稳定 |
| B.不用浓硝酸与铜屑反应来制取硝酸铜,说明浓硝酸具有挥发性 |
| C.足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+ |
| D.锌与稀硝酸反应得不到氢气,说明稀硝酸能使锌钝化 |