实验室常采用点滴板来完成部分实验,既可节约药品,又便于观察实验现象。图中所示的实验现象描述正确的是( )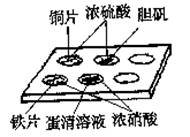
①装有铜片的孔穴中溶液呈蓝色
②装有胆矾的孔穴中固体的颜色变浅
③装有铁片的孔穴中溶液呈浅绿色
④装有铁片的孔穴中溶液呈浅黄色
⑤装有蛋清溶液的孔穴中溶液呈黄色
| A.①④ | B.②③ | C.①⑤ | D.②⑤ |
将盛有12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积是
| A.1.2mL | B.2.4mL | C.3.6mL | D.3mL |
下列说法错误的是( )
| A.制造水泥和玻璃都用到的原料是CaCO3 |
| B.为了调节水泥的硬化速度,制造水泥时需要加入石膏 |
| C.当水泥、沙子与水调成水泥浆时,水泥浆对皮肤有腐蚀作用,这是因为水泥浆呈较强的碱性 |
| D.水泥、玻璃、陶瓷都是混合物,具有较高的熔点 |
我们看到的普通玻璃一般呈淡绿色,这是因为在制造玻璃的过程中加入了( )
| A.氧化钴 | B.二价铁 | C.氧化亚铜 | D.氧化镁 |
用图所示装置进行实验,下列对实验现象的解释不合理的是( )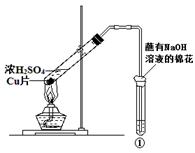
| | ①中试剂 | ①中现象 | 解 释 |
| A | Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成白色BaSO3沉淀 |
| B | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
| C | 紫色石蕊溶液 | 溶液变红 | SO2与水反应生成酸 |
| D | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了。则液体A和气体B的组合不可能是下列的:
| A.氢氧化钠溶液、二氧化碳 | B.硝酸银溶液、氯化氢 |
| C.水、氨气 | D.水、一氧化碳 |
下列有关说法正确的是( )
| A.实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
| B.为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解 |
C.N2(g)+3H2(g) 2NH3(g) ΔH<0,其他条件不变时升高温度,平衡时氢气转化率增大 2NH3(g) ΔH<0,其他条件不变时升高温度,平衡时氢气转化率增大 |
| D.吸热反应“TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的ΔS<0 |
将液体A滴入烧瓶与气体B充分反应,打开夹子,可发现试管内的水立刻沸腾了,则液体A和气体B的组合不可能是( )
| A.水、氯化氢 |
| B.硫酸、氨气 |
| C.氢氧化钠溶液、二氧化硫 |
| D.氢氧化钠溶液、一氧化碳 |
将过量的CO2分别通入①CaC12溶液;②Na2SiO3溶液;③Ca(C1O)2溶液;④饱和Na2CO3溶液。最终溶液中有白色沉淀析出的是
| A.①②③④ | B.②④ | C.①②③ | D.②③ |
CuSO4是一种重要的化工原料,其有关制备途径如图所示。下列说法不正确的是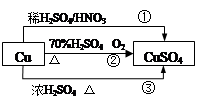
(已知:2Cu O2
O2 2H2SO4=2CuSO4
2H2SO4=2CuSO4 2H2O)
2H2O)
| A.相对于途径①、③,途径②更好地体现了绿色化学思想 |
| B.途径③中,1mol Cu与足量浓硫酸反应会产生64g SO2气体 |
C.途径①所用混酸中H2SO4与HNO3物质的量之比最好为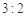 |
D.1mol Cu分别按照途径②、③中,被还原的H2SO4的质量之比为 |