下列有关物质性质的应用正确的是( )
| A.液氨汽化时要吸收大量的热,可用作制冷剂 |
| B.二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 |
| C.生石灰能与水反应,可用来干燥氯气 |
| D.氯化铝是一种电解质,可用于电解法制铝 |
下列有关说法,错误的是( )
| A.氮氧化物、二氧化硫都是形成酸雨的主要物质 |
| B.工业合成氨及用NH3制化肥(NH4)2SO4都属于氮的固定 |
| C.一定条件下,镁能与一些非金属氧化物反应,铝能与一些金属氧化物反应 |
| D.玻璃中含有硅酸钠和二氧化硅 |
硝酸铜是一种重要的工业产品,化学上有很多方法可以制取硝酸铜:①将铜溶于硝酸中 ②先将铜与O2反应生成CuO,再溶于硝酸中 ③将铜溶于N2O4的乙酸乙酯(溶剂,不参加反应)溶液中生成硝酸铜和一氧化氮。下列认识或判断中错误的是( )
| A.方法③是最经济和环保的 |
| B.方法①中,若从经济和环保的角度考虑,用稀硝酸比用浓硝酸好 |
| C.方法②需要消耗能源,对环境不产生污染 |
| D.方法③中N2O4既是氧化剂又是还原剂 |
利用常温下氨与氯气能发生置换反应的性质,氯碱工业生产中用来检查氯气是否泄漏,其模拟装置如图所示。下列有关说法中错误的是( )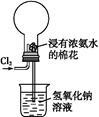
| A.烧瓶中立即出现白烟 |
| B.烧瓶中立即出现红棕色气体 |
| C.烧瓶中发生的反应表明常温下氨气有还原性 |
| D.烧瓶中还发生了化合反应 |
某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种气体。现将此无色混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,气体很快变为红棕色。下列对原混合气体成分的判断中正确的是( )
| A.肯定只有SO2和NO | B.肯定有Cl2、O2和NO2 |
| C.可能有Cl2和O2 | D.肯定只有NO |
下列相关化学与生活、生产的叙述错误的是( )
| A.用作“钡餐”的物质主要成分是硫酸钡 |
| B.采用催化设施,将汽车尾气中CO和NO转化为无害气体 |
| C.常温下,可以用铁制容器来盛装冷的浓硫酸 |
| D.SO2具有氧化性,可用于漂白纸浆 |
以下每个选项中的两组物质都能反应,且能放出同一种气体的是( )
| A.铜与稀硫酸,铜与浓硫酸 |
| B.铁与稀硫酸,铁与浓硫酸 |
| C.硫化钠与稀硫酸,亚硫酸钠与稀硫酸 |
| D.硫化钠与稀硫酸,硫化钠与稀盐酸 |
如图是某煤发电厂处理废气的装置示意图。下列说法错误的是( )
| A.使用此废气处理装置可减少酸雨的形成 |
| B.装置内发生的反应有化合、分解、置换和氧化还原反应 |
C.整个过程的反应可表示为:2SO2+2CaCO3+O2 2CaSO4+2CO2 2CaSO4+2CO2 |
| D.可用酸性高锰酸钾溶液检验废气处理是否达标 |
将SO2分别通入下列4种溶液中,有关说法正确的是( )
| A.试管a中实验可以证明SO2具有漂白性 |
| B.试管b中溶液褪色,说明SO2具有强氧化性 |
| C.试管c中能产生白色沉淀,说明SO2具有还原性 |
| D.试管d中能产生白色沉淀,该沉淀完全溶于稀硝酸 |
某同学用下列装置制备并检验Cl2的性质。下列说法正确的是( )

| A.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗 |
| B.Ⅱ图中:量筒中发生了加成反应 |
| C.Ⅲ图中:生成蓝色的烟 |
| D.Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成 |