科学家从化肥厂生产的(NH4)2SO4中检验出组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO42-和N2H44+两种离子形式存在,植物的根系极易吸收N4H44+,但它遇到碱时,会生成一种形似白磷的N4分子。N4分子不能被植物吸收。下列有关说法不正确的是( )
| A.N4和N2互为同素异形体 |
| B.14N与14C互为同位素 |
| C.N4H4(SO4)2不能与草木灰混合使用 |
| D.8NH3+4C5OH=N4+4C5NH2+6H2+4H2O,此反应中每生成5.6 g N4时转移1.2 mol电子 |
有a、b、c、d、e五种气体,现进行下列实验:
| (1)a和b混合 | 气体变红棕色 |
| (2)c和d混合 | 产生白烟 |
| (3)c和e分别通入少量溴水中 | 溴水都变成无色透明的液体 |
| (4)b和e分别通入氢硫酸中 | 都产生淡黄色浑浊 |
则a、b、c、d、e依次可能是( )
A.O2、NO、HCl、NH3、CO2
B.O2、NO、NH3、HCl、SO3
C.NO、O2、NH3、HCl、SO2
D.HCl、CO2、NH3、H2S、CH4
NaCl是一种化工原料,可以制备一系列物质,如图所示。下列说法正确的是( )。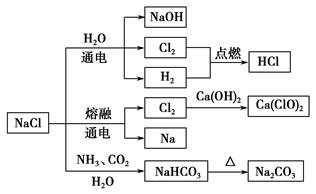
| A.25 ℃时,NaHCO3在水中的溶解度比Na2CO3的大 |
| B.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
| C.常温下干燥的Cl2能用钢瓶贮运,所以Cl2不与铁反应 |
| D.图示转化反应都是氧化还原反应 |
某同学用下列装置制备并检验Cl2的性质。下列说法正确的是 ( )。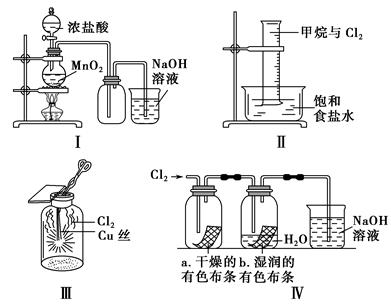
| A.Ⅰ图中:如果MnO2过量,浓盐酸就可被全部消耗 |
| B.Ⅱ图中:量筒中发生了加成反应 |
| C.Ⅲ图中:生成蓝色的烟 |
| D.Ⅳ图中:湿润的有色布条能退色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成 |
某化学兴趣小组利用MnO2和浓HCl及如图装置制备Cl2。下列分析中不正确的是 ( )。
| A.A中可用分液漏斗代替长颈漏斗 |
| B.A中缺少加热装置 |
| C.B中盛放的NaOH溶液可以净化Cl2 |
| D.D中的导管口若连接倒置漏斗可防止倒吸 |
下列推断正确的是
| A.绿色化学的核心是应用化学原理对环境污染进行治理 |
| B.硅是地壳中含量位居第二的元素,玛瑙、光导纤维的主要成分为SiO2 |
| C.加碘食盐中加人的是碘单质,可防止甲状腺肿大疾病 |
| D.要除去衣服上的顽固污渍,均可将衣服泡在漂白液中 |
下列有关氨水的说法正确的是( )
| A.氨水有弱碱性,能使湿润的红色石蕊试纸变蓝 |
| B.氨水是弱碱,化学式是 NH3?H2O |
| C.氨水中存在三种分子和四种离子 |
| D.氨很容易液化,液化时放热,液化后得到氨水 |
下列表述正确的是
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中放置是否变质可以先加硝酸溶液,再加氯化钡溶液来检验
③锌与稀硝酸反应可以得到氢气
④足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
⑤ 浓硫酸滴到纸张上变黑,说明浓硫酸具有吸水性
⑥二氧化硫和二氧化氮都能形成酸雨,酸雨的pH等于5.6
| A.①③④ | B.①② | C.① | D.①②⑤⑥ |
氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性,下列叙述中不正确的是
| A.灼热的铜丝在Cl2中剧烈地燃烧,产生棕黄色的烟 |
| B.氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸 |
| C.漂白粉是混合物,其有效成分是次氯酸钙 |
| D.漂白粉放入稀盐酸中会降低漂白效果 |