下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到FeCl3溶液中 ②过量NaOH溶液和明矾溶液混合 ③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2O2投入FeCl2溶液中
| A.只有①④ | B.只有③ | C.只有②③ | D.只有①③④ |
FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存
在,下列判断不正确的是( )
| A.加入KSCN溶液一定不变红色 |
| B.溶液中一定含Fe2+ |
| C.溶液中一定含Cu2+ |
| D.剩余固体中一定含铜 |
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示。则溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为( )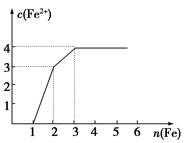
| A.1∶1∶1 | B.1∶3∶1 |
| C.3∶3∶8 | D.1∶1∶4 |
将一浅绿色溶液,置于空气中,变黄色。将此黄色溶液逐滴滴入沸水中,
形成一种红褐色胶体,下列说法中错误的是( )
| A.该浅绿色溶液中含有Fe2+,在空气中被氧化为Fe3+ |
| B.欲检验该黄色溶液中是否含有未被氧化的Fe2+,向其中滴加KSCN溶液 |
| C.配制该浅绿色溶液,要向其中加少量酸与铁粉,目的是为了防止Fe2+的水解与氧化 |
| D.欲检验浅绿色溶液中是否含有Fe3+,滴入KSCN溶液,看是否变红色 |
下列离子方程式中正确的是( )
| A.用FeCl3溶液腐蚀铜制印刷电路板:Fe3++Cu=Fe2++Cu2+ |
| B.NH4HCO3溶液和过量的NaOH溶液相混合:HCO3—+OH-=CO32—+H2O |
| C.向Fe2(SO4)3的酸性溶液中通入足量H2S:Fe3++H2S=FeS↓+2H+ |
| D.FeI2溶液中通入Cl2至I-恰好完全被氧化:2I-+Cl2=I2+2Cl- |
在FeCl3、CuCl2混合溶液中,加入一定量的铁屑,反应完全后将固体滤出,下列说法中正确的是( )
| A.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+ |
| B.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,可能含有Cu2+和Fe3+ |
| C.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe3+和Fe2+,一定不含Cu2+ |
| D.若滤出的固体中含有铁和铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+和Fe3+ |
红珊瑚栖息于200~2000 m的海域,产于台湾海峡、南中国海,它与琥珀、珍珠被统称为有机宝石。在中国,珊瑚是吉祥的象征,一直用来制作珍贵的工艺品。红珊瑚是无数珊瑚虫分泌的石灰质大量堆积形成的干支状物,其红色是因为在海底长期积淀某种元素,该元素是( )
| A.Na | B.Fe | C.Si | D.Cu |
下列关于铁的叙述正确的是( )
①铁能被磁铁吸引,但纯铁易锈蚀 ②在人体的血红蛋白中含有铁元素 ③不能通过化合反应生成FeCl2和Fe(OH)3 ④铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧 ⑤铁与硝酸反应的产物仅是Fe(NO3)3
| A.①③ | B.②④ | C.②⑤ | D.③⑤ |