右图模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是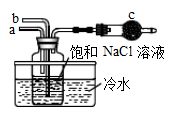
| A.a通入CO2,然后b通入NH3,c中放碱石灰 |
| B.b通入NH3,然后a通入CO2,c中放碱石灰 |
| C.a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉 |
| D.b通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉 |
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下图转化关系。下列有关物质的推断正确的是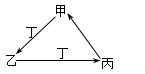
| A.若甲为焦炭,则丁可能是O2 |
| B.若甲为Fe,则丁可能是Cl2 |
| C.若甲为AlCl3,则丁可能是NH3 |
| D.若甲为NaHCO3,则丁可能是HCl |
下列有关物质性质、应用的说法正确的是
| A.小苏打可与酸反应,可用作治疗胃酸过多的药剂 |
| B.氯化铝是电解质,可电解其水溶液获得金属铝 |
| C.SO2具有漂白性,可用于将银耳漂白为“雪耳” |
| D.二氧化硅具有导电性,可用于生产光导纤维 |
下列实验和结论均正确的是
| 选项 | 操作 | 解释或结论 |
| A | 向某溶液中加入NaOH溶液,出现白色沉淀 | 溶液中一定含有Mg2+ |
| B | 在饱和的SO2溶液中通入NO2气体,溶液的pH变小 | SO2具有还原性 |
| C | 某酸HX稀释100倍后,pH增加2 | HX是强酸 |
| D | 配制FeSO4溶液时,应加入过量铁粉和稀硫酸 | 溶液中不断产生FeSO4 |
下列陈述中,Ⅰ、Ⅱ都正确且两者间具有因果关系的一组是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | FeCl3溶液能腐蚀Cu | Fe的金属性强于Cu |
| B | Na2O2使酚酞溶液变红 | Na2O2是碱性氧化物 |
| C | Cl2可部分与水反应 | 用排饱和食盐水法收集Cl2 |
| D | 浓H2SO4可干燥NO和SO2 | NO和SO2还原性都弱 |
下列实验操作能达到预期实验目的的是
| | 实验目的 | 实验操作 |
| A | 鉴别Al3+和Fe3+ | 分别加入过量NaOH溶液 |
| B | 比较Fe和Cu的金属活动性 | 分别加入浓硝酸 |
| C | 证明品红溶液褪色的原因是通入了SO2 | 将褪色后的溶液再加热 |
| D | 分离乙酸乙酯和乙酸 | 加饱和NaOH溶液,蒸馏 |
X、Y、P、Q四种短周期元素,元素X在地壳中含量最高,充有元素Y单质蒸气的灯透雾能力强,常用于道路和广场的照明,Q的最外层电子数与其电子总数比为3:8,P的单质常用作电脑的芯片材料。
| A.元素Y、P的简单氢化物中化学键类型相同 |
| B.原子半径:X>Y |
| C.最高价氧化物的水化物酸性:P<Q |
| D.X、Q两元素的最高正化合价相同 |
化学与科学、技术、社会、环境密切相关。下列说法正确的是
| A.盐酸与氢氧化钠的反应可自发进行,因此可用作原电池反应原理 |
| B.“地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |
| C.铁粉、硅胶是食品包装中常用的干燥剂 |
| D.铝表面可生成一层致密的氧化物薄膜,因此可用铝容器盛装稀硫酸 |
下列实验的现象与对应结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| B | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
| C | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
| D | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
固体粉末X中可能含有Fe、Fe2O3、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3中的若干种。为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下: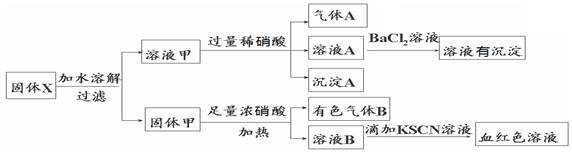
根据上述实验,以下说法正确的是
| A.气体A一定只是NO |
| B.由于在溶液A中加入BaCl2溶液有沉淀产生,因此可以判断溶液中含有K2SO3 |
| C.若向固体甲中加入足量浓盐酸,再加KSCN溶液,没有血红色,则证明原混合物中一定没有Fe2O3 |
| D.溶液甲中一定含有K2SiO3、可能含有KAlO2、MgCl2 |