下列应用不涉及氧化还原反应的是
| A.工业上利用N2和H2合成氨,实现人工固氮 |
| B.实验室用NH4Cl和Ca(OH)2制备NH3 |
| C.用FeCl3溶液作为“腐蚀液”刻蚀电路铜板 |
| D.用Na2O2作潜水艇的供氧剂 |
下列变化需要加入适当的氧化剂才能完成的是 ( )
| A.CuO→Cu | B.HNO3→NO |
| C.Na2SO3→SO2 | D.FeCl2→FeCl3 |
24 mL浓度为0.05 mol·L-1的Na2SO3溶液(已知硫元素最高价为+6价),恰好与20 mL浓度为0.02 mol·L-1的K2Cr2O7(Cr元素最高价为+6价)溶液完全反应,则元素Cr在被还原的产物中的化合价是( )。
| A.+6 | B.+3 | C.+2 | D.0 |
黄铜矿(CuFeS2)常用于提炼金属铜。黄铜矿焙烧过程中所发生的反应比较复杂,其中主要反应之一的化学方程式为2CuFeS2+O2
 +2FeS+SO2(已配平),则下列关于该反应的说法错误的是( )。
+2FeS+SO2(已配平),则下列关于该反应的说法错误的是( )。
| A.方框中的物质应为CuS |
| B.该反应的部分产物可用于硫酸工业 |
| C.反应中SO2既是氧化产物又是还原产物 |
| D.反应中若有1 mol SO2生成,则一定有4 mol电子发生转移 |
下列叙述正确的是( )。
| A.阳离子只有氧化性,阴离子只有还原性 |
| B.含氧酸可作氧化剂而无氧酸不能 |
| C.在8NH3+3Cl2=N2+6NH4Cl反应中氧化剂与还原剂物质的量之比是2∶3 |
| D.已知还原性:Fe2+>Br-,可知反应2Fe3++2Br-=2Fe2++Br2不易进行 |
Na2FeO4是一种高效多功能水处理剂,一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2 +O2↑。下列对此反应的说法中,不正确的是( )
+O2↑。下列对此反应的说法中,不正确的是( )
| A.方框中的物质为Na2SO4 |
| B.Na2O2既是氧化剂,又是还原剂 |
| C.Na2FeO4既是氧化产物,又是还原产物 |
| D.2 mol FeSO4发生反应时,反应中共转移8 mol电子 |
某反应的反应物与生成物有:K2Cr2O7、KCl、CrCl3、Cl2、HCl、H2O,已知氧化性:K2Cr2O7>Cl2,则下列说法不正确的是
( )
| A.Cl2是该反应的氧化产物 |
| B.氧化剂和被氧化的还原剂的物质的量之比为1∶14 |
| C.当转移0.2 mol电子时,被氧化的还原剂的物质的量为0.2 mol |
| D.由该反应可知还原性:HCl>CrCl3 |
LiNi0.25Co0.75O2是锂离子电池的一种高性能的二元正极活性材料,其制备原理可表示为4Ni0.25Co0.75(OH)2+4LiOH+O2=4LiNi0.25Co0.75O2+6H2O(已知Ni与Co的化合价均有+2和+3)。下列说法不正确的是( )
| A.Ni0.25Co0.75(OH)2中Ni的化合价是+2 |
| B.LiNi0.25Co0.75O2中Co的化合价是+3 |
| C.该反应中LiOH是还原剂 |
| D.该反应中O2是氧化剂 |
下列说法正确的是( )
| A.常温常压下,22.4 L氯气与足量镁粉充分反应,转移的电子数为2NA |
| B.化合反应均为氧化还原反应 |
| C.电解NaCl溶液得到22.4 L H2(标准状况),理论上需要转移NA个电子(NA表示阿伏加德罗常数) |
| D.易燃试剂与强氧化性试剂分开放置并远离火源 |
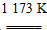 aTiCl4+cCO
aTiCl4+cCO Ti+2MgCl2
Ti+2MgCl2