将以下4份溶液分别置于下图的装置中,其它条件相同时,灯泡最亮的是
| A.100mL 1mol/L的盐酸 |
| B.100mL 2mol/L的蔗糖溶液 |
| C.100mL 1mol/L的醋酸溶液 |
| D.30mL 1mol/L的CaCl2溶液 |
下列表示对应化学反应的离子方程式正确的是
| A.NaHCO3溶液与醋酸溶液反应:HCO3- + H+="==" CO2↑+H2O |
| B.氯化铝溶液与过量氨水反应:Al3+ + 4OH-="==" AlO2-+ 2H2O |
| C.Na2O2溶于水产生O2:Na2O2+H2O ="==" 2Na++2OH-+O2↑ |
D.NaOH溶液与氯化铵溶液在加热下反应:NH4++OH- NH3↑+H2O NH3↑+H2O |
在碱性条件下,溶液无色且可以大量共存的离子组是
| A.K+、Ca2+、Cl-、HCO3- | B.Cu2+、Cl-、Na+、SO42- |
| C.Ba2+、Na+、Cl-、NO3- | D.Na+、Mg2+、NO3-、Cl- |
某溶液中可能含有H+、NH4+、Mg2+、Fe3+、Al3+、SO42-、HCO3—等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随加入NaOH溶液的体积变化如图所示,下列说法正确的是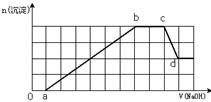
| A.d点溶液中含有的溶质只有Na2SO4 |
| B.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1 |
| C.ab段发生的离子反应为:Al3++3OH-= Al(OH)3↓,Mg2++2OH—= Mg(OH)2↓ |
| D.原溶液中含有的阳离子必定有H+、NH4+、Al3+,但不能肯定Mg2+和Fe3+中的哪一种 |
下列离子方程式书写正确的是
| A.铵明矾[NH4Al(SO4)2·12H2O]溶液中加入过量Ba(OH)2溶液: Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| B.H218O中投入Na2O2固体:2H218O + 2Na2O2 = 4Na+ + 4OH- + 18O2↑ |
| C.碳酸氢钙溶液中加过量澄清石灰水:Ca2+ + OH- + HCO3- = CaCO3↓ + H2O |
D.碳酸钠的水解反应:CO32-+ H3O+ HCO3-+ H2O HCO3-+ H2O |
下列各反应对应的离子方程式正确的是
| A.向100 mL 0.12 mol/L的Ba(OH)2溶液中通入0.02 mol CO2:OH-+CO2 → HCO3- |
| B.向Ca(OH)2溶液中加入过量的NaHCO3溶液:Ca2+ + 2OH-+2HCO3- → CaCO3↓+ CO32-+ 2H2O |
| C.向0.2 mol溴化亚铁溶液中通入0.2 mol氯气:2Fe2++4Br-+3Cl2 → 2Fe3++6Cl-+2Br2 |
| D.硫酸氢钠与氢氧化钡两种溶液反应后pH恰好为7:H++SO42-+Ba2++OH-→ BaSO4↓+H2O |
为使溶液中的3种阳离子A+、B2+、C3+逐一沉淀分离,将含有A+、B2+、C3+离子的水溶液进行如下实验, 
关于三种离子的判断正确的是
| A.Ag+、Fe2+、Al3+ | B.NH4+、Fe2+、Fe3+ |
| C.Ag+、Cu2+、Fe3+ | D.Ag+、Cu2+、Al3+ |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.无色溶液中:K+、Na+、Cu2+、SO42- |
| B.c(H+)/c(OH-)=1×10-14的溶液:K+、Na+、Cl-、SiO32- |
| C.由水电离出的C(OH-)=1×10-12 mol·L-1的溶液:NH4+、HCO3-、Na+、Cl- |
| D.c(OH-)=10-13 mol·L-1的溶液中:Al3+、NO3-、I-、Cl- |
水溶液中能大量共存的一组离子是
| A.Al3+、Cl—、A1O2—、SiO32— |
| B.H+、Na+、S2—、ClO— |
| C.K+、Mg2+、SO42—、MnO4ˉ |
| D.Fe3+、Ca2+、SCN—、NO3— |