下列离子方程式正确的是
| A.用Fe除去FeCl2溶液中的少量的FeCl3杂质:Fe+Fe3+=2Fe2+ |
B.实验室制取NO2:Cu+4H++2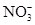 =Cu2++2NO2↑+2H2O =Cu2++2NO2↑+2H2O |
C.硫酸溶液与氢氧化钡溶液混合:H++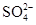 +Ba2++OH-=BaSO4↓+H2O +Ba2++OH-=BaSO4↓+H2O |
D.向氯化铝溶液通足量氨气:Al3++4NH3+4H2O=4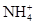 +[Al(OH)4]- +[Al(OH)4]- |
下列各组离子在指定分散系中一定能大量共存的是
A.pH=0的溶液中: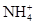 、Fe3+、 、Fe3+、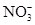 、Cl- 、Cl- |
B.明矾溶液中:Na+、Mg2+、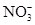 、 、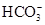 |
| C.氢氧化铁胶体中:H+、K+、Cl-、S2- |
D.使酚酞变红的溶液中:Na+、Ba2+、Cl-、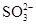 |
下列离子方程式正确的是
A.HCO3-水解的离子方程式:HCO3-+H2O CO32-+H3O+ CO32-+H3O+ |
| B.漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3- |
| C.过量的SO2通入NaOH溶液中:SO2—+2OH—=SO32—+H2O |
D.新制氢氧化铜和乙醛反应:CH3CHO+2Cu(OH)2+OH- CH3COO-+Cu2O↓+3H2O CH3COO-+Cu2O↓+3H2O |
常温下,下列溶液中各组离子一定大量共存的是
| A.使甲基橙呈红色的溶液中:Na+、AlO2—、NO3—、CO32— |
| B.c(ClO-)=1.0 mol·L-1溶液:Na+、SO32-、S2-、Cl- |
| C.含有0.1 mol·L-1 HCO3-的溶液:Na+、Fe3+、NO3-、C6H5O- |
D.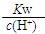 =0.1 mol·L-1的溶液:Na+、K+、CO32-、NO3— =0.1 mol·L-1的溶液:Na+、K+、CO32-、NO3— |
下列表示对应化学反应的离子方程式正确的是
A.氯气溶于水:Cl2+H2O H++Cl-+HClO H++Cl-+HClO |
| B.铝溶于氢氧化钠溶液:Al+2OH-+H2O=AlO2-+2H2↑ |
| C.少量的CO2 通入氨水中:CO2+NH3?H2O=NH4++HCO3- |
| D.用醋酸溶液除去水垢:2H++CaCO3=Ca2++CO2↑+H2O |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.使甲基橙变红的溶液:Fe2+、K+、SO42-、NO3- |
| B.加入铝粉产生氢气的溶液:Na+、K+、SO42-、Cl- |
| C.0.1 mol·L-1NaAlO2溶液:Al3+、Na+、Cl-、NO3- |
| D.水电离出的c(H+)=10-12 mol·L-1的溶液:Na+、K+、NH4+、CO32- |
下列能正确表示相应过程的离子方程式的是( )
| A.纯碱显碱性的原因:CO32-+ 2 H2O = H2CO3 + 2 OH- |
B.稀盐酸和稀氢氧化钠溶液反应的中和热△H=-57.3 kJ/mol,则稀硫酸与稀氢氧化钾溶液发生反应的热化学方程式表示为: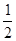 H2SO4(l)+ KOH(l) = H2SO4(l)+ KOH(l) = 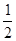 K2SO4 (l)+ H2O(l) △H=-57.3 kJ/mol K2SO4 (l)+ H2O(l) △H=-57.3 kJ/mol |
| C.明矾溶液中滴加氢氧化钡溶液至沉淀的物质的量最大: 2 Al3+ +3 SO42-+3 Ba2+ +6 OH- =" 2" Al(OH)3 ↓+ 3 BaSO4 ↓ |
D.铜和浓硫酸混合加热:2H2SO4(浓)+Cu SO2↑+Cu2+ +SO42-+2 H2O SO2↑+Cu2+ +SO42-+2 H2O |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.能使酚酞变红的溶液:Na+、Ba2+、NO3-、Cl- |
| B.含有0.1 mol·L-1 Fe3+的溶液中:K+、Mg2+、I-、SO42- |
| C.能溶解Al(OH)3的溶液:NH4+、K+、SO42-、HCO3- |
| D.c(Al3+)="0.5" mol·L-1的溶液中:Na+、K+、[Al(OH)4]-、SO42- |
在下列给定条件的溶液中,一定能大量共存的离子组是
| A.澄清透明溶液:H+、Na+、SO42-、C6H5O- |
| B.常温下Kw/c(H+)=0.1 mol/L的溶液:K+、Na+、SiO32-、NO3- |
| C.铁片加入产生气泡的溶液:Na+、NH4+、I-、NO2- |
| D.NaHCO3溶液:K+、Na+、SO42-、Al3+ |
某含Na+的溶液中可能含有NH4+、Fe3+、Br—、CO32—、I—、SO32—。取样,滴加足量氯水,有气泡产生,溶液呈橙色;向橙色溶液中加BaCl2溶液或淀粉均无现象。为确定该溶液的组成,还需进行的实验有
| A.取样,滴加硫氰化钾溶液 |
| B.取样,加氯水和CCl4,振荡 |
| C.取样,加足量盐酸加热,湿润的品红试纸检验气体 |
| D.取样,加足量的熟石灰加热,湿润的红色石蕊试纸检验气体 |