下列离子方程式正确的是
| A.lmol Cl2通入含有2mol FeI2的溶液中:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
| B.澄清石灰水与少量小苏打溶液混合:Ca2++OH-+ HCO3-=CaCO3↓+H2O |
| C.AlCl3溶液中加入过量氨水:Al3++4 OH-= AlO-2+2H2O |
| D.向银氨溶液中加入足量的盐酸:[Ag(NH3)2]++OH-+3H+= Ag++2NH4++ H2O |
下列离子方程式正确的是
| A.水玻璃长时间放置在空气中:SiO32-+CO2+H2O=H2SiO3↓+HCO3- |
| B.硫酸铜溶液显酸性:Cu2++2H2O=Cu(OH)2↓+2H+ |
C.用石墨电极电解饱和食盐水:2H++2Cl-  H2↑+Cl2↑ H2↑+Cl2↑ |
| D.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全: |
下列离子方程式不正确的是
| A.向AgCl悬浊液中加入Na2S溶液:2AgCl+S2-=Ag2S+2Cl- |
| B.向NaHCO3溶液中加入NaOH溶液:HCO3-+OH-= CO32-+H2O |
| C.向Ba(OH)2溶液中加入稀H2SO4:Ba2++OH-+H++ SO42-= BaSO4↓+ H2O |
| D.向Cu粉中加入过量的浓HNO3:Cu+4 H++ 2NO3-= Cu2++2 NO2↑+2H2O |
已检测出pH=1的某未知溶液中含有Al3+和 ,若检验此溶液中是否大量存在以下6种离子:①ClO-②
,若检验此溶液中是否大量存在以下6种离子:①ClO-② ③Fe2+④K+⑤
③Fe2+④K+⑤ ⑥Cl-,其中不必检验就能加以否定的离子是
⑥Cl-,其中不必检验就能加以否定的离子是
| A.①②⑥ |
| B.②③④ |
| C.①③⑤ |
| D.④⑤⑥ |
下列离子或分子在溶液中能大量共存,通入SO2后仍能大量共存的一组是
【选项】
| A.K+、Ca2+、Br-、Cl- | B.NH3·H2O、SO32-、K+、Na+ |
| C.Fe2+、Na+、K+、NO3- | D.Na+、Mg2+、Cl-、ClO- |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.1.0mol·L-1的KNO3溶液:Cl-、SO42-、H+、Fe2+ |
| B.c(H+)=1.0×10-12mol·L-1的溶液:K+、Na+、CH3COO-、Br- |
| C.甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl- |
D.与铝反应产生大量氢气的溶液:Na+、K+、CO32-、 |
下列图示与对应的叙述不相符的是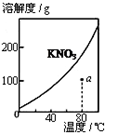
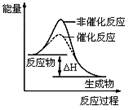
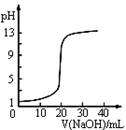

图1 图2 图3 图4
| A.图1表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 |
| B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| C.图3表示0.1000mol?L-1NaOH溶液滴定20.00mL0.1000mol?L-1醋酸溶液得到的滴定曲线 |
| D.图4 表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化 |
下列各组离子一定能大量共存的是
| A.加入铝粉有氢气产生的溶液中Na+、K+、SO42-、Cl-、HCO3- |
| B.含有大量硝酸根离子的溶液中H+、Fe2+、SO42-、Cl- |
| C.常温下,c(H+)/c(OH-) = 1×10-10的溶液中NH4+、K+、Ca2+、Cl- |
| D.常温下pH=1的溶液中:MnO4-、NO3-、SO42-、Na+、Fe3+ |

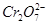 +H+—→CO2↑+Cr3++H2O,当这个方程式配平后,H+的化学计量数为
+H+—→CO2↑+Cr3++H2O,当这个方程式配平后,H+的化学计量数为